题目内容
(1)氯化铝水溶液呈酸性的原因是 (用离子方程式表示).
(2)5.6g金属铁(相对原子质量56)与足量的氯气反应,同时放出热量Q KJ.写出此反应热化学方程式: .
(2)5.6g金属铁(相对原子质量56)与足量的氯气反应,同时放出热量Q KJ.写出此反应热化学方程式:
考点:盐类水解的原理,热化学方程式
专题:基本概念与基本理论
分析:(1)氯化铝为强酸弱碱盐,铝离子水解导致溶液呈酸性;
(2)n(Fe)=
=0.1mol,0.1mol铁在氯气中燃烧放出QkJ热量,则1molFe在氯气中燃烧放出10QkJ热量.
(2)n(Fe)=
| 5.6g |
| 56g/mol |
解答:
解:(1)氯化铝为强酸弱碱盐,铝离子水解导致溶液呈酸性,水解方程式为Al3++3H3O?Al(OH)3+3H+,
故答案为:Al3++3H3O?Al(OH)3+3H+;
(2)n(Fe)=
=0.1mol,0.1mol铁在氯气中燃烧放出QkJ热量,则1molFe在氯气中燃烧放出10QkJ热量,其热化学反应方程式为Fe(s)+
Cl2(g)=FeCl3(s)△H=-10QkJ/mol,
故答案为:Fe(s)+
Cl2(g)=FeCl3(s)△H=-10QkJ/mol.
故答案为:Al3++3H3O?Al(OH)3+3H+;
(2)n(Fe)=
| 5.6g |
| 56g/mol |
| 3 |
| 2 |
故答案为:Fe(s)+
| 3 |
| 2 |
点评:本题考查了盐类水解、热化学反应方程式的书写,根据“谁强谁显性、谁弱谁水解”确定溶液酸碱性,书写水解方程式时不能写“↑”或“↓”符号,注意热化学溶液方程式中焓变与计量数有关,为易错点.

练习册系列答案
相关题目
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质,已知,它们可以发生如下反应:甲+乙→丁+己,甲+丙→戊+己;0.1mol/L丁溶液的pH为13(25℃).它们满足如图转化关系,下列说法正确的是( )
| A、Z元素在周期表中的位置为二周期第ⅥA族 |
| B、原子半径:W>Z>Y>X |
| C、1mol甲与足量的乙完全反应共转移了2mol电子 |
| D、1L 0.1mol/L戊溶液中阴离子总的物质的量小于0.1mol |
用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A、1mol醛基中含有电子的数目为16NA |
| B、1L pH=1的水溶液中含氢离子数目为NA |
| C、每生成1mol O2,电子转移数目一定是4NA |
| D、30g二氧化硅晶体中含共价键的数目为2NA |
下列说法正确的是( )
| A、糖类、油脂、蛋白质都能够发生水解反应 |
| B、酯在碱性条件下的水解反应叫皂化反应 |
| C、煤的干馏、石油的分馏都是化学变化 |
| D、在船身装上锌块利用的是牺牲阳极的阴极保护法 |
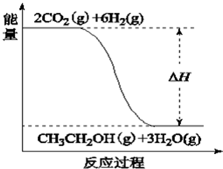 A、B、C、D是中学化学常见的四种物质,它们的转化关系为:A+B═C+D
A、B、C、D是中学化学常见的四种物质,它们的转化关系为:A+B═C+D