题目内容
下列说法正确的是( )
| A、硅和石墨都是重要的半导体材料 |
| B、SO2、NO2、CO2都会导致酸雨的形成 |
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理不同 |
| D、氢能是清洁能源,工业上用电解水法制大量氢气符合节能减排理念 |
考点:硅和二氧化硅,清洁能源,盐类水解的应用,二氧化硫的化学性质
专题:化学应用
分析:A.用于制造半导体材料的元素既具有金属性又具有非金属性,在金属与非金属交界处附近元素可以用来做半导体材料;
B.根据酸雨的形成原因分析;
C.明矾中含有Al3+,水解呈酸性,生成Al(OH)3;漂白粉[有效成分为Ca(ClO)2]溶于水,在空气中CO2作用下可生成碳酸钙和次氯酸,次氯酸有强氧化性具有杀菌消毒作用;
D.从减少能源危机和节能减排方面分析判断.
B.根据酸雨的形成原因分析;
C.明矾中含有Al3+,水解呈酸性,生成Al(OH)3;漂白粉[有效成分为Ca(ClO)2]溶于水,在空气中CO2作用下可生成碳酸钙和次氯酸,次氯酸有强氧化性具有杀菌消毒作用;
D.从减少能源危机和节能减排方面分析判断.
解答:
解:A.Si在金属元素与非金属元素的分界线附近的元素,可作半导体材料,石墨是电的良导体,故A错误;
B.因酸雨的形成是由于SO2、NO2而引起的,与CO2无关,故B错误;
C.明矾中含有Al3+,水解呈酸性,生成Al(OH)3,Al(OH)3能吸附水中悬浮的杂质;漂白粉中的次氯酸钙[Ca(ClO)2]与水和空气中的CO2反应生成了次氯酸(HClO)和另一种物质,次氯酸具有杀菌消毒作用,两者的作用原理不同,故C正确;
D.氢能燃烧生成水是清洁能源,但工业上用电解水法制大量氢气,消耗大量电能,增大能源危机,故D错误;
故选C.
B.因酸雨的形成是由于SO2、NO2而引起的,与CO2无关,故B错误;
C.明矾中含有Al3+,水解呈酸性,生成Al(OH)3,Al(OH)3能吸附水中悬浮的杂质;漂白粉中的次氯酸钙[Ca(ClO)2]与水和空气中的CO2反应生成了次氯酸(HClO)和另一种物质,次氯酸具有杀菌消毒作用,两者的作用原理不同,故C正确;
D.氢能燃烧生成水是清洁能源,但工业上用电解水法制大量氢气,消耗大量电能,增大能源危机,故D错误;
故选C.
点评:本题主要考查了半导体材料、酸雨的形成、自来水的净化和杀菌消毒、节能减排等知识,题目难度不大,平时注意相关知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应中,不属于氧化还原反应的是( )
| A、3Cl2+6KOH═5KCl+KClO3+3H2O |
| B、2FeBr2+3Cl2═2FeCl3+2Br2 |
| C、SnCl4+2H2O═SnO2+4HCl |
| D、Ca(OH )2+CO2═CaCO3↓+H2O |
准确量取21.00mL KMnO4溶液,可选用的仪器是( )
| A、25mL量筒 |
| B、25mL酸式滴定管 |
| C、25mL碱式滴定管 |
| D、有刻度的50mL烧杯 |
下列叙述正确的是( )
| A、糖类、蛋白质都属于天然高分子化合物 |
| B、强紫外线灼伤人体皮肤属于皮肤蛋白质的变性 |
| C、纤维素和淀粉的组成都可用(C6H10O5)n表示,它们互为同分异构体 |
| D、向鸡蛋清溶液中分别加入饱和(NH4)2SO4和CuSO4溶液都能使之聚沉,其原理相同 |
已知两种物质发生化学反应的微观示意图如图(一种小球代表一种原子,原子间的短线代表原子的结合),下列说法正确的是( )
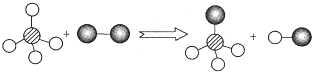

| A、图示中共有3种分子 |
| B、说明化学反应中原子不可分 |
| C、该图示不符合质量守恒定律 |
| D、该反应属于置换反应 |
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质,已知,它们可以发生如下反应:甲+乙→丁+己,甲+丙→戊+己;0.1mol/L丁溶液的pH为13(25℃).它们满足如图转化关系,下列说法正确的是( )
| A、Z元素在周期表中的位置为二周期第ⅥA族 |
| B、原子半径:W>Z>Y>X |
| C、1mol甲与足量的乙完全反应共转移了2mol电子 |
| D、1L 0.1mol/L戊溶液中阴离子总的物质的量小于0.1mol |
下列物质中,不含有硅酸盐的是( )
| A、水玻璃 | B、硅芯片 |
| C、粘土 | D、平板玻璃 |
 汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,机动车废气排放已成为城市大气污染的重要来源.
汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,机动车废气排放已成为城市大气污染的重要来源.