题目内容
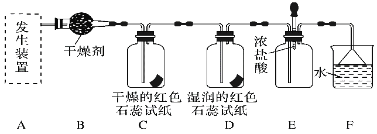
【题目】如图是中学化学实验中常见的制备气体并进行某些物质的检验和性质实验的装置,A是制备气体的装置,C、D、E、F中盛装的液体可能相同,也可能不同。试回答:

(1)如果A中的固体物质是碳,分液漏斗中盛装的是浓硫酸,试写出发生的化学反应方程式:____,若要检验生成的产物,则B、C、D、E、F中应分别加入的试剂为__、__、__、__、__,E中试剂和C中相同,E中试剂所起的作用__,B装置除可检出某产物外,还可起到__作用。
(2)若进行上述实验时在F中得到10.0 g固体,则A中发生反应转移的电子数为__个。
【答案】C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 无水CuSO4 品红溶液 足量的酸性KMnO4溶液 品红溶液 澄清石灰水 检验SO2是否已被除尽 防倒吸 2.408×1023
CO2↑+2SO2↑+2H2O 无水CuSO4 品红溶液 足量的酸性KMnO4溶液 品红溶液 澄清石灰水 检验SO2是否已被除尽 防倒吸 2.408×1023
【解析】
(1)浓硫酸和木炭粉在加热条件下发生反应生成二氧化碳、二氧化硫和水;检验水用无水硫酸铜,检验二氧化硫使用品红溶液,检验二氧化碳用澄清石灰水,为了防止二氧化硫对二氧化碳的检验产生干扰,要用足量的酸性KMnO4溶液吸收剩余的二氧化硫;
(2)依据原子个数守恒计算反应碳的物质的量,再依据碳的物质的量计算转移电子数目。
(1)浓硫酸和木炭粉在加热条件下发生反应生成二氧化碳、二氧化硫和水,反应的化学方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;因检验二氧化硫和二氧化碳均用到溶液,会带出水蒸气影响水的检验,则应先检验水,则B中试剂为无水硫酸铜,B装置除可检验反应生成的水外,还可起到防倒吸的作用;检验二氧化硫使用品红溶液,检验二氧化碳用澄清石灰水,二氧化硫对二氧化碳的检验产生干扰,则应先检验二氧化硫,并除去二氧化硫后,再检验二氧化碳,则C中试剂为品红溶液,检验二氧化硫,D中试剂为足量的酸性KMnO4溶液,吸收除去二氧化硫,E中试剂为品红溶液,检验SO2是否已被除尽,F中试剂为澄清石灰水,检验二氧化碳,故答案为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;因检验二氧化硫和二氧化碳均用到溶液,会带出水蒸气影响水的检验,则应先检验水,则B中试剂为无水硫酸铜,B装置除可检验反应生成的水外,还可起到防倒吸的作用;检验二氧化硫使用品红溶液,检验二氧化碳用澄清石灰水,二氧化硫对二氧化碳的检验产生干扰,则应先检验二氧化硫,并除去二氧化硫后,再检验二氧化碳,则C中试剂为品红溶液,检验二氧化硫,D中试剂为足量的酸性KMnO4溶液,吸收除去二氧化硫,E中试剂为品红溶液,检验SO2是否已被除尽,F中试剂为澄清石灰水,检验二氧化碳,故答案为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;无水CuSO4;品红溶液;足量的酸性KMnO4溶液;品红溶液;澄清石灰水;检验SO2是否已被除尽;防倒吸;
CO2↑+2SO2↑+2H2O;无水CuSO4;品红溶液;足量的酸性KMnO4溶液;品红溶液;澄清石灰水;检验SO2是否已被除尽;防倒吸;
(2)F中得到的10.0g固体为碳酸钙,10.0g碳酸钙的物质的量为0.1mol,由碳原子个数守恒可知,0.1mol碳与浓硫酸共热反应生成0.1mol二氧化碳转移0.4mol电子,则转移的电子数目为0.4mol×6.02×1023mol—1=2.408×1023个,故答案为:2.408×1023。

【题目】下表是元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题.
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)可作半导体材料的元素是 ______(填元素符号);气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐的元素是 _____(填名称);
(2)第三周期中离子半径最小的是___________(填离子符号);
(3)① ~ ⑨的最高价氧化物的水化物中:酸性最强的是 __________(填化学式);碱性最强的是________(填化学式),它与⑥的最高价氧化物的水化物反应的离子方程式为__________。
(4)⑧、⑨可形成A2B2型的化合物,分子中二者均满足8电子稳定结构,则其电子式为_________________。
【题目】下表是元素周期表的一部分,按要求完成各小题。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)元素①的元素符号:_______________
(2)元素⑧的单质电子式_______________
(3)元素⑤的原子结构示意图______________
(4)化学性质最不活泼的元素______(填元素符号,下同),非金属性最强的元素是________。金属性最强的单质_______。
(5)①③⑤三种元素的最高价氧化物水化物中,碱性最强的 _____(填化学式,下同)。①③⑤三种元素的原子半径由大到小的顺序为_____________。
(6)某元素的最高价氧物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为 _____,与氢氧化钠溶液反应的化学方程式_____。