��Ŀ����
����Ŀ��ij��ѧ��ȤС��Ϊ����ȡ��̽���������ʣ�������װ��(���ּг�װ������ȥ)����ʵ�顣��֪����ȡ�����ķ�Ӧԭ��Ϊ2NH4Cl��Ca(OH)2![]() CaCl2��2NH3����2H2O
CaCl2��2NH3����2H2O

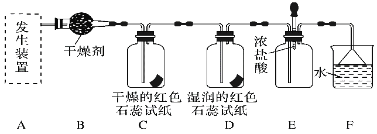
[ʵ��̽��]
��1����������ԭ����ʵ������ȡ����Ӧѡ����ͼ��________(�����)����װ�ý���ʵ�顣
��2��Bװ���еĸ������ѡ��________(������ʯ��������Ũ������)��
��3������ͨ��C��Dװ��ʱ����ֽ��ɫ�ᷢ���仯����________(����C������D��)��
��4��Fװ���е���©����������___________________________________��
��5��ijͬѧ�ð����͵μӷ�̪��ˮ����Ȫʵ�飬������ƿ�ڲ�����ɫ��Ȫ������˵����������________����(�����)��
a����ԭ�� b����������ˮ c����ˮ��Ӧ���ɼ�������
���𰸡�a ��ʯ�� D ������ bc
��������
��1����������ԭ����ʵ������ȡ����Ϊ��������������ȡ���壬��ѡ�� aװ�ã��ʴ�Ϊ��a��
��2������Ϊ�������壬�����ü�ʯ�Ҹ���ʴ�Ϊ����ʯ�ң�
��3��������ˮ��Ӧ���ɵ�һˮ�ϰ��������������������ˮ��Һ�ʼ��ԣ�ʹʪ��ĺ�ɫʯ����ֽ������������ͨ��C��Dװ��ʱ����ֽ��ɫ�ᷢ���仯����ʪ��ĺ�ɫʯ����ֽ����D���ʴ�Ϊ��D��
��4��Fװ���е���©���������Ƿ�ֹ�������ʴ�Ϊ����������
��5�������͵μӷ�̪��ˮ������ɫ��Ȫ��˵��������������ˮ������ˮ��Ӧ���ɼ������ʣ��ʴ�Ϊ��bc��

����Ŀ����ȩ��ľ�ļӹ���ҽҩ�ȷ�������Ҫ��;���״�ֱ�������ǹ�ҵ�Ϻϳɼ�ȩ���·������Ʊ������漰����Ҫ��Ӧ���£�
��ӦI��CH3OH(g)![]() HCHO(g)+H2(g) ��H1=+85.2kJ��mol��1
HCHO(g)+H2(g) ��H1=+85.2kJ��mol��1
��ӦII��CH3OH(g)+1/2O2(1)![]() HCHO(g)+H2O(g) ��H2
HCHO(g)+H2O(g) ��H2
��ӦIII��H2(g)+1/2O2(g)![]() H2O(g) ��H3=��241.8kJ��mol��1
H2O(g) ��H3=��241.8kJ��mol��1
����Ӧ��
��ӦIV��CH3OH(g)+O2(g)![]() CO(g)+2H2O(g) ��H4=��393.0kJ��mol��1
CO(g)+2H2O(g) ��H4=��393.0kJ��mol��1
��1�����㷴Ӧ���ķ�Ӧ����H2=____________________________________________��
��2��750K�£��ں����ܱ������У�������ӦCH3OH(g)![]() HCHO(g)+H2(g��������ʼѹǿΪP0���ﵽƽ��ת����Ϊ������ƽ��ʱ����ѹǿPƽ=___________(�ú�P0������ʽ�ӱ�ʾ)����P0=101kPa�������=50.0%�����㷴Ӧƽ�ⳣ��Kp=___________kPa(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������������������Ӧ)��
HCHO(g)+H2(g��������ʼѹǿΪP0���ﵽƽ��ת����Ϊ������ƽ��ʱ����ѹǿPƽ=___________(�ú�P0������ʽ�ӱ�ʾ)����P0=101kPa�������=50.0%�����㷴Ӧƽ�ⳣ��Kp=___________kPa(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������������������Ӧ)��
��3��Na2CO3�Ǽ״������Ƽ�ȩ�Ĵ��������о�ָ��������Ӧ�IJ��ֻ������£�
����i��CH3OH��H+��CH2OH
����������CH2OH����H+HCHO
����������CH2OH��3��H+CO
����iv����H+��H��H2
��ͼ��ʾһ���������¶ȶ�̼���ƴ��������ܵ�Ӱ�죬�ش��������⣺
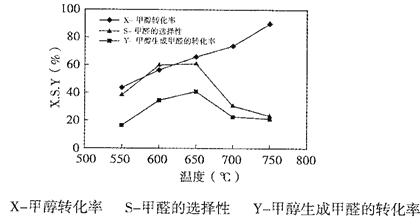
�ٴ�ƽ��ǶȽ���550��-650���״����ɼ�ȩ��ת�������¶����ߵ�ԭ��___________��
�ڷ�Ӧ����i�Ļ��___________(����>����<������=��)CH3OH(g)![]() HCHO(g)+H2(g)��ܡ�
HCHO(g)+H2(g)��ܡ�
��650��~750������Ӧ����ii������___________(����>������<������=��)��Ӧ�����������ʡ�
��4�������Ǵ�����ȩ��ˮ��һ�ֹ��գ��������ʿ��÷���v=0.0423c(mg��L��1��h��1)��ʾ(����cΪ��ȩŨ��)���±�Ϊ�����¼�ȩ��Ũ���洵��ʱ��仯���ݡ�
Ũ��(mg/L) | 10000 | 8000 | 4000 | 2000 | 1000 |
����ʱ��(h) | 0 | 7 | 23 | 39 | 55 |
��ȩŨ��Ϊ2000mg/Lʱ���䴵������v=___________ mg��L��1��h��1�������ϱ����ݣ���ʼŨ��Ϊ10000mg/L������ȩŨ�Ƚ�Ϊ5000mg/L������ʱ��Ϊ___________h��
����Ŀ����ѧ��Ӧ������������ѧ��Ӧ���п����̶ȵ���������������ijͬѧ�ⶨ��ѧ��Ӧ���ʲ�̽����Ӱ�����ص�ʵ�顣

��.�ⶨ��ѧ��Ӧ����
��ͬѧ������ͼװ�òⶨ��ѧ��Ӧ���ʡ�
��1��д���÷�Ӧ�����ӷ���ʽ ___________________________________________________;Ϊ��֤ʵ��ȷ�ԡ��ɿ��ԣ����ø�װ�ý���ʵ��ǰӦ�Ƚ��еIJ�����______________������ͼ��ʾ��ʵ����Ʒ�������⣬����Ҫ��һ��ʵ��������__________________��
��2������2 minʱ�ռ���224 mL(������ɱ�״��)���壬�ɼ������2 min��H���ķ�Ӧ���ʣ����òⶨֵ��ʵ��ֵƫС����ԭ����____________________________________________��
��3���Լ����ⶨ�÷�Ӧ�Ļ�ѧ��Ӧ���ʵ�����������_______________________________________________(дһ��)��
��.Ϊ̽�ֻ�ѧ��Ӧ���ʵ�Ӱ�����أ�ij̽��С����HNO3�����ʯ��Ӧ������������С�ķ������о�Ӱ�췴Ӧ���ʵ����ء�����HNO3Ũ��Ϊ1.00 mol��L-1��2.00 mol��L-1������ʯ��ϸ������ֿ������ֹ��ʵ���¶�Ϊ298 K��308 K��ÿ��ʵ��HNO3������Ϊ25.0 mL������ʯ����Ϊ10.00 g��
��4�����������ʵ����Ʊ�������ʵ��Ŀ��һ���������Ӧ��ʵ���ţ�
ʵ���� | T/K | ����ʯ��� | HNO3Ũ��/mol��L-1 | ʵ��Ŀ�� |
�� | 298 | �ֿ��� | 2.00 | ������ʵ��������̽��HNO3Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죻 ������ʵ������______̽���¶ȶԸ÷�Ӧ���ʵ�Ӱ�죻 ������ʵ������______̽������ʯ��֡�ϸ���Ը÷�Ӧ���ʵ�Ӱ�졣 |
�� | _______ | �ֿ��� | ______ | |
�� | ____ | ___ | 2.00 | |
�� | 298 | ________ | _____ |
����Ŀ���ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
�¶ȣ��棩 | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��1����д����ҵ�ϳɰ��Ļ�ѧ����ʽ_________��
�����ϱ����ݿ�֪�÷�ӦΪ���ȷ�Ӧ��������_________��
�������ϣ�Ϊ������ƽ��ʱH2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��_________��������ţ�
a. ����ѹǿ b. ʹ�ú��ʵĴ���
c. �����¶� d. ��ʱ����������е�NH3
��2��ԭ����H2��ͨ����ӦCH4(g)+H2O(g)![]() CO(g)+3H2(g)��ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO(g)+3H2(g)��ȡ����֪�÷�Ӧ�У�����ʼ������е�![]() �㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��
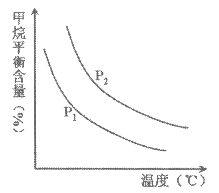
��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ�ǣ�P1_____P2��������������=��������������
�ڸ÷�ӦΪ________��Ӧ��������������������������
��3��ԭ����H2����ͨ����ӦCH4(g)+H2O(g)![]() CO(g)+3H2(g)��ȡ��T��ʱ�����ݻ��̶�Ϊ5L�������г���1molˮ������1mol CO����Ӧ��ƽ����CO��Ũ��Ϊ0.08 mol��L-1
CO(g)+3H2(g)��ȡ��T��ʱ�����ݻ��̶�Ϊ5L�������г���1molˮ������1mol CO����Ӧ��ƽ����CO��Ũ��Ϊ0.08 mol��L-1
��ƽ��ʱCO��ת����Ϊ_________��
�ڸ��¶��·�Ӧ��ƽ�ⳣ��KֵΪ_________��


