题目内容
【题目】氢氧燃料电池如图所示,a、b均为惰性电极。下列叙述不正确的是
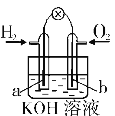
A.a极是负极,该电极上发生氧化反应
B.b极反应是O![]() +4OH
+4OH![]() -4e
-4e![]() =2H
=2H![]() O
O
C.总反应方程式为2H![]() +O
+O![]() =2H
=2H![]() O
O
D.氢氧燃料电池是一种具有应用前景的绿色电源
【答案】B
【解析】
A. 氢氧燃料电池工作时,通入氢气的一极(a极)为电池的负极,发生氧化反应,故A正确;
B. 通入氧气的一极(b极)为电池的正极,发生还原反应,正极反应为:O2+4e+2H2O=4OH,故B错误;
C. 氢氧燃料电池的电池总反应方程式与氢气在氧气中燃烧的化学方程式一致,都是2H2+O2=2H2O,故C正确;
D. 氢氧燃料电池总反应方程式为2H2+O2=2H2O,电池工作时生成水,无污染,是一种具有应用前景的绿色电源,故D正确;
故选B。

 名校课堂系列答案
名校课堂系列答案【题目】室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=![]() mol/L
mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)
【题目】下列说法正确的是( )
A.标准状况下,向![]()
![]() 的醋酸溶液中加入醋酸钠晶体,若混合液的
的醋酸溶液中加入醋酸钠晶体,若混合液的![]() ,则该溶液中
,则该溶液中![]()
B.根据下表中有关共价键的键能:
共价键 |
|
|
|
|
键能 | 348 | 610 | 413 | 436 |
可以计算出反应:![]()
![]()
![]()
![]() 的
的![]()
C.一定量的复盐![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,在某一时刻,反应的离子方程式可能是
溶液,在某一时刻,反应的离子方程式可能是![]()
D.已知:![]() ,
, ,向该温度下的饱和
,向该温度下的饱和![]() 溶液中加入一定量的硫酸钠或氯化钡固体后使
溶液中加入一定量的硫酸钠或氯化钡固体后使![]() 增大
增大