题目内容
14.通过煤的干馏能获得甲苯等基本化工原料,利用甲苯并通过以下路线可合成M(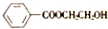 )和N(
)和N(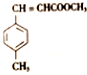 )
)路线一:
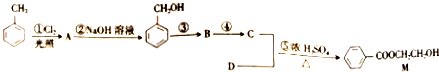
(1)物质A的核磁共振氢谱有4个峰,峰面积之比是1:2:2:2.
(2)属于取代反应的有(填序号):①②⑤.
(3)写出D与足量Na反应的化学方程式:2Na+HOCH2CH2OH→NaOCH2CH2ONa+H2↑.
路线二:
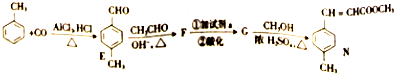
已知:HCHO+CH2CHO$\stackrel{OH-△}{→}$CH2=CHCHO+H2O
(4)写出G中所含官能团(除苯环外)的名称碳碳双键、羧基.
(5)试剂a可选用下列中的CD.
A.溴水 B.酸性KMnO4溶液 C.新制Cu(OH)2悬浊液 D.银氨溶液
(6)R(
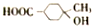 )是E经多步反应的产物,与R共有相同官能团且官能团都直接连在六元环上,则满足上述条件R的共同异构体还有18种(不考虑立体异构).
)是E经多步反应的产物,与R共有相同官能团且官能团都直接连在六元环上,则满足上述条件R的共同异构体还有18种(不考虑立体异构).(7)N在一定条件下可以生成高聚物P,P的结构简式为
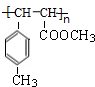 .
.
分析 路线一:甲苯与氯气在光照条件发生侧链取代反应生成A,A发生卤代烃水解反应生成苯甲醇,则A为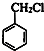 ,苯甲醇系列反应得到C,由M的结构逆推可知,C为
,苯甲醇系列反应得到C,由M的结构逆推可知,C为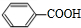 ,D为HOCH2CH2OH,苯甲醇发生催化氧化生成B为
,D为HOCH2CH2OH,苯甲醇发生催化氧化生成B为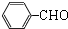 ,苯甲醛发生氧化反应生成苯甲酸;
,苯甲醛发生氧化反应生成苯甲酸;
路线二:对比甲苯与E的结构,可知甲苯与CO发生加成反应生成E,E与乙醛发生信息中反应生成F为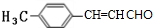 ,F转化得到G,由N的结构逆推可知G为
,F转化得到G,由N的结构逆推可知G为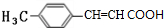 ,试剂a为新制氢氧化铜或银氨溶液.
,试剂a为新制氢氧化铜或银氨溶液.
解答 解:路线一:甲苯与氯气在光照条件发生侧链取代反应生成A,A发生卤代烃水解反应生成苯甲醇,则A为 ,苯甲醇系列反应得到C,由M的结构逆推可知,C为
,苯甲醇系列反应得到C,由M的结构逆推可知,C为 ,D为HOCH2CH2OH,苯甲醇发生催化氧化生成B为
,D为HOCH2CH2OH,苯甲醇发生催化氧化生成B为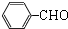 ,苯甲醛发生氧化反应生成苯甲酸.
,苯甲醛发生氧化反应生成苯甲酸.
(1)物质A为 ,核磁共振氢谱有4个峰,峰面积之比是1:2:2:2,故答案为:4;1:2:2:2;
,核磁共振氢谱有4个峰,峰面积之比是1:2:2:2,故答案为:4;1:2:2:2;
(2)反应①②⑤属于取代反应,反应②③属于氧化反应,故答案为:①②⑤;
(3)D与足量Na反应的化学方程式:2Na+HOCH2CH2OH→NaOCH2CH2ONa+H2↑,故答案为:2Na+HOCH2CH2OH→NaOCH2CH2ONa+H2↑;
路线二:对比甲苯与E的结构,可知甲苯与CO发生加成反应生成E,E与乙醛发生信息中反应生成F为 ,F转化得到G,由N的结构逆推可知G为
,F转化得到G,由N的结构逆推可知G为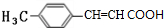 ,试剂a为新制氢氧化铜或银氨溶液.
,试剂a为新制氢氧化铜或银氨溶液.
(4)G为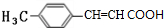 ,所含官能团(除苯环外)的名称:碳碳双键、羧基,
,所含官能团(除苯环外)的名称:碳碳双键、羧基,
故答案为:碳碳双键、羧基;
(5)试剂a是将醛基氧化为羧基,溴水能与碳碳双键发生加成反应,酸性KMnO4溶液可以氧化碳碳双键,新制Cu(OH)2悬浊液与银氨溶液氧化醛基,不影响碳碳双键,故选:CD;
(6)与R(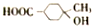 )共有相同官能团且官能团都直接连在六元环上,含有三个侧链-CH3、-COOH、-OH,三个基团分别连接不同碳原子时,当CH3、-COOH处于邻位,-OH有4种位置,当CH3、-COOH处于间位,-OH有4种位置,当CH3、-COOH处于对位,-OH有2种位置,其中2个基团连接同一碳原子时,另外的基团有3种位置,两个基团的组合有3种(包含R),故R的同分异构体有4+4+2+3×3-1=18种,
)共有相同官能团且官能团都直接连在六元环上,含有三个侧链-CH3、-COOH、-OH,三个基团分别连接不同碳原子时,当CH3、-COOH处于邻位,-OH有4种位置,当CH3、-COOH处于间位,-OH有4种位置,当CH3、-COOH处于对位,-OH有2种位置,其中2个基团连接同一碳原子时,另外的基团有3种位置,两个基团的组合有3种(包含R),故R的同分异构体有4+4+2+3×3-1=18种,
故答案为:18;
(7)N( )在一定条件发生加聚反应生成高聚物P,P的结构简式为
)在一定条件发生加聚反应生成高聚物P,P的结构简式为  ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断,充分利用有机物的结构与反应条件进行推断,需要学生熟练掌握官能团的性质与转化,(6)中同分异构体的书写为易错点,难度中等.

 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案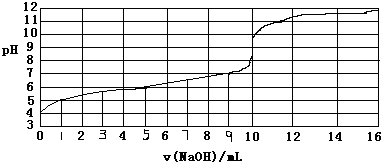
| A. | 此实验可以选用酚酞作指示剂 | |
| B. | 弱酸HA的浓度约为1×10-4mol/L | |
| C. | 根据已知条件,弱酸HA的电离常数(Ka)不能计算 | |
| D. | 当NaOH体积为9ml时,恰好完全中和反应 |
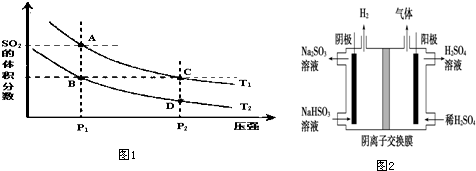
(1)比较K值的大小,K1<K2(填>、=、<).
(2)下列说法正确的是CD
A.A、C两点的正反应速率:A>C
B.A、C两点SO2气体的浓度:A>C
C.B、C两点的气体的平均相对分子质量:B=C
D.由状态D到状态C,可以用加热的方法
(3)在500℃时,若保持容积不变,每隔一定时间就对该容器内的物质进行分析,得到如下表的部分数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(SO2)/mol | 2.00 | 0.60 | |||
| n(SO3)/mol | 0.00 | 0.80 | 1.8 | 1.8 |
②该条件下反应的平衡常数K的值为368.2(精确到小数点后一位).
(4)工业上用Na2SO3吸收尾气中的SO2使之转化为NaHSO3,再用图2装置电解(惰性电极)NaHSO3制取H2SO4,该电解池阴极的总电极反应式2HSO3-+2e-═SO32-+H2↑,阳极室除生成硫酸外,还有少量的SO2 和O2生成.则阳极发生的副反应的电极反应式为2SO32-+4e-═2SO2↑+O2↑,该工艺中可循环利用的物质是Na2SO3、H2SO4、SO2(填化学式).
| A. | 葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体 | |
| B. | C5H12有3种同分异构体 | |
| C. | 氨基酸、淀粉均属于高分子化合物 | |
| D. | 碳原子之间只以单键相结合的链烃为烷烃 |
| A. | 可能含有Ag+、Al3+、NH4+ | B. | 一定不含Cl-,可能含有NO3- | ||
| C. | 一定不含NH4+、AlO2-、CO32- | D. | 可能含有Fe3+,一定不含Fe2+ |
| A. | 酸性 | B. | 碱性 | C. | 中性 | D. | 无法判断 |
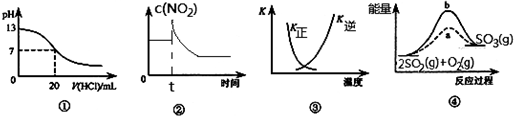
| A. | 图①表示25℃时,用0.1 mol•L-1盐酸滴定10 mL 0.05 mol•L-1 Ba(OH)2溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②表示充有NO2的恒温密闭容器在t时刻增大压强时,c(NO2)随时间的变化 | |
| C. | 图③中曲线表示反应N2 (g)+3 H2(g)═2NH3(g)△H<0,正、逆反应的平衡常数K随温度的变化 | |
| D. | 图④中a、b曲线分别表示反应2SO2(g)+O2(g)═2SO3(g)△H<0使用(a)和未使用(b)催化剂时,应过程中的能量变化 |
| A. | 苯制备环己烷 | B. | 甲烷与氯气制备一氯甲烷 | ||
| C. | 铜和浓硝酸为原料生产硝酸铜 | D. | 苯与硝酸反成制备硝基苯 |