题目内容
取20 mL NaOH溶液平均分成两份,分别放入A、B两支试管中。向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如下表所示:
| 盐酸体积(单位:mL) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| A产生CO2的体积 | 0 | 0 | 0 | 0 | 0 | 22.4 | 44.8 | 44.8 | 44.8 |
| B产生CO2的体积 | 0 | 0 | 22.4 | 44.8 | 67.2 | 89.6 | x | x | x |
(1)少量CO2与NaOH溶液反应的离子方程式 ,
过量CO2与NaOH溶液反应的化学方程式 ;
(2)试管A中通入CO2后所得溶液的溶质为 ;
(3)原NaOH溶液的物质的量浓度为 mol/L;
(4)滴加70mL盐酸时,A、B产生CO2的体积均为最大值,则x= mL。
(1)CO2+2OH-=CO32-+H2O;CO2+NaOH=NaHCO3(2)NaOH、Na2CO3(3)0.7(4)112
解析试题分析:(1)CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H20,故少量CO2与NaOH溶液反应的离子方程式CO2+2OH-=CO32-+H2O;过量CO2与NaOH溶液反应的化学方程式CO2+NaOH=NaHCO3(2)当n(CO2):n(NaOH)≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成生成NaHCO3,CO2有剩余;当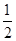 <n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;当n(CO2):n(NaOH)≤
<n(CO2):n(NaOH)<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;当n(CO2):n(NaOH)≤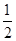 ,反应按②进行,等于
,反应按②进行,等于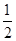 ,时,CO2、NaOH恰好反应生成Na2CO3;小于
,时,CO2、NaOH恰好反应生成Na2CO3;小于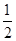 时,生成Na2CO3,NaOH有剩余;,A中通入CO2后所得溶液的溶质为Na2CO3,NaOH(3)加入70ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液.根据氯离子、钠离子守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.07ml×0.1mol/L=0.007mol,所以c(NaOH)=
时,生成Na2CO3,NaOH有剩余;,A中通入CO2后所得溶液的溶质为Na2CO3,NaOH(3)加入70ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液.根据氯离子、钠离子守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.07ml×0.1mol/L=0.007mol,所以c(NaOH)= 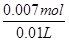 =0.7mol/L,故答案为:0.7mol/L;(4)由曲线B可知从20ml到70ml为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(CO2)=n(HCl)=(0.07ml-0.02ml)×0.1mol/L=0.005mol,所以CO2气体体积为0.005mol×22.4L/mol=0.112L=112mL,故答案为112。
=0.7mol/L,故答案为:0.7mol/L;(4)由曲线B可知从20ml到70ml为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(CO2)=n(HCl)=(0.07ml-0.02ml)×0.1mol/L=0.005mol,所以CO2气体体积为0.005mol×22.4L/mol=0.112L=112mL,故答案为112。
考点:化学反应方程式的有关计算

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案