题目内容
闪锌矿(主要成份为ZnS)是含锌主要矿物之一,空气中高温加热闪锌矿生成ZnO和SO2。ZnO用于冶炼金属锌,SO2可制亚硫酸盐或硫酸。回答下列问题(以下计算保留2位小数)
(1)取1.56 g闪锌矿样品,在空气中高温加热(杂质不反应),充分反应后,冷却,得到残留
固体的质量为1.32 g,样品中含硫化锌的质量分数是_________。
(2)取1.95 g锌加入到12.00 mL 18.4 mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000 mL,取出15.00 mL,以酚酞为指示剂,用0.25 mol/L的NaOH溶液中和余酸,耗用NaOH溶液的体积为21.70 mL。
①反应后溶液中多余的硫酸是____________ mol。
②通过计算确定浓硫酸被还原的产物是________________________。
(3)将标况下4.48 L SO2气体慢慢通入200 mL一定浓度NaOH溶液中,SO2气体全部被吸收,将反应后的溶液在空气中小心蒸干(不考虑酸式盐的分解),得到不超过两种物质的无水晶体26.8g。通过计算确定所得晶体的成分与物质的量。
(1)0.93
(2)0.18mol (2分)还原产物是S。(2分) (3)
(3)



解析试题分析:(1)设闪锌矿中ZnS的质量为x,杂质为y
2ZnS+3O2="2" ZnO+2SO2
x/97 x/97
有
解得x=1.455g,y=0.105g,所以样品中w(ZnS)=1.455g÷1.56g×100%=93%
(2)设浓硫酸被还原的产物中S的化合价为x。56、根据题意过量的硫酸用碱滴定,则过量的硫酸n(H2SO4)= n(NaOH)×1000/15="0.25" mol/L×0.02170 L×1000/15=0.1808mol,所以反应的硫酸n(H2SO4)="18.4" mol/L×0.012L-0.1808mol=0.04mol,又反应后溶液为硫酸锌,所以n(ZnSO4)= n(Zn)="1.95" g÷65g/mol=0.03mol,所以作酸的硫酸n(H2SO4)= n(ZnSO4)=0.03mol,做氧化剂硫酸n(H2SO4)=0.04mol-0.03mol=0.01mol,因为Zn反应0.03mol失去0.06mol电子,所以根据得失电子守恒,(+6-x) ×0.01mol=0.06mol,解得x=0,所以还原产物中S的化合价为0价,还原产物为S单质。
(3)n(SO2)=0.2mol,通入未知浓度的NaOH溶液,若NaOH溶液过量则所得溶液为Na2SO3 、NaOH;若恰好完全反应则所的溶液为Na2SO3 溶液;若SO2稍过量则所得溶液为Na2SO3 、NaHSO3 ;若SO2过量恰好完全被吸收则生成NaHSO3 溶液;(1)若所得溶液为Na2SO3 、NaOH:则有n(Na2SO3)= n(SO2)=0.2mol,则m(Na2SO3)=25.2g<26.8g,蒸干后若得到的是Na2SO3 、NaOH时,满足条件,此时m(NaOH)= 26.8g-25.2g=1.6g,即n(NaOH)=0.04mol.(2)若恰好完全反应所得溶液为Na2SO3 :因n(Na2SO3)= n(SO2)=0.2mol,则m(Na2SO3)=25.2g<26.8g,蒸干后必有部分Na2SO3 被氧化为Na2SO4 ;设n(Na2SO3)=x,n(Na2SO4)=y,则有:
解得x=0.1mol,y=0.1mol即n(Na2SO3)=0.1mol,n(Na2SO4)= 0.1mol.(3)若SO2稍过量所得溶液为Na2SO3 、NaHSO3 :当蒸干后固体全为Na2SO3时,m(Na2SO3)=25.2g<26.8g,所以蒸干溶液后所得晶体不可能是Na2SO3 、NaHSO3 组合;当蒸干后固体全为Na2SO4 时,m(Na2SO4)="0.2mol×142g/mol=28.4g" >26.8g,所以蒸干后不可能全是Na2SO4,可以是Na2SO4 和NaHSO3或者是Na2SO4 和NaHSO4 ,因此有
设n(NaHSO3)=x,n(Na2SO4)=y
解得x=0.042mol,y=0.158mol即n(NaHSO3)= 0.042mol,n(Na2SO4)= 0.158mol
设n(NaHSO4)=x,n(Na2SO4)=y
解得x=0.073mol,y=0.127mol即n(NaHSO3)= 0.073mol,n(Na2SO4)= 0.127mol。(4)若SO2过量恰好被吸收所得溶液为NaHSO3 :则蒸干后所得固体无论是NaHSO3 还是NaHSO4 或者二者混合,都不可能。
考点:本题考查的是氧化还原计算、金属与酸反应计算、多元酸的酸性氧化物与碱反应的计算。

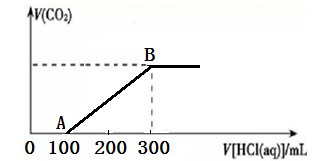
取20 mL NaOH溶液平均分成两份,分别放入A、B两支试管中。向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如下表所示:
| 盐酸体积(单位:mL) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| A产生CO2的体积 | 0 | 0 | 0 | 0 | 0 | 22.4 | 44.8 | 44.8 | 44.8 |
| B产生CO2的体积 | 0 | 0 | 22.4 | 44.8 | 67.2 | 89.6 | x | x | x |
(1)少量CO2与NaOH溶液反应的离子方程式 ,
过量CO2与NaOH溶液反应的化学方程式 ;
(2)试管A中通入CO2后所得溶液的溶质为 ;
(3)原NaOH溶液的物质的量浓度为 mol/L;
(4)滴加70mL盐酸时,A、B产生CO2的体积均为最大值,则x= mL。
天然碱的组成可以用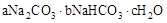 (a、b、c为整数)表示。现有A、B两种不同的天然碱样品,分别进行如下实验以确定其化学式。
(a、b、c为整数)表示。现有A、B两种不同的天然碱样品,分别进行如下实验以确定其化学式。
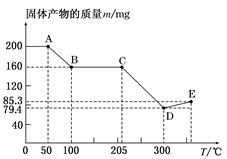
将质量为31.0 g的天然碱A于300℃加热分解至完全(300℃时Na2CO3不分解),产生CO2 2.24 L(标准状况)和水5.4 g。
(1)天然碱A的化学式中: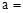
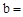

已知:Na2CO3与稀盐酸的反应分下列两步进行:
Na2CO3+HCl NaCl+NaHCO3 NaHCO3+HCl
NaCl+NaHCO3 NaHCO3+HCl NaCl+CO2↑+H2O
NaCl+CO2↑+H2O
将质量为12.45 g的天然碱B溶于水,逐滴滴加某浓度的稀盐酸,产生气体的体积与加入盐
酸的体积(标准状况)的关系如下表所示:
| 盐酸体积(mL) | 20 | 40 | 60 | 80 |
| 产生气体体积(mL) | 0 | 560 | 1680 | 2520 |
(2)由表中数据可推测加入50mL盐酸时,产生气体的体积为 mL(标准状况);盐酸的浓度为 mol/L;天然碱B的化学式为: 。
(3)若取一定质量的天然碱B加入到30mL该浓度的盐酸中,请写出产生气体体积V(mL,标准状况)与天然碱B质量W(g) 之间的关系式。
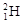 和
和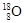 组成的水分子的物质的量 mol,其中含中子数为 mol,电子数为 个。
组成的水分子的物质的量 mol,其中含中子数为 mol,电子数为 个。 MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有 mol HCl被氧化,转移电子的物质的量为 mol,产生的Cl 2在标准状况下的体积为 L。
MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有 mol HCl被氧化,转移电子的物质的量为 mol,产生的Cl 2在标准状况下的体积为 L。