题目内容
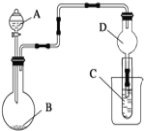
【题目】我国某科研团队设计了一种新型能量存储/转化装置(如下图所示)。闭合K2、断开K1时,制氢并储能;断开K2、闭合K1时,供电。下列说法错误的是
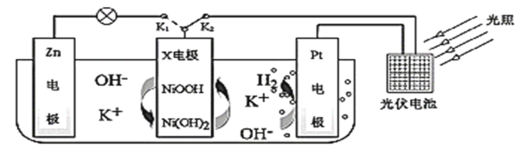
A.制氢时,溶液中K+向Pt电极移动
B.制氢时,X电极反应式为![]()
C.供电时,Zn电极附近溶液的pH升高
D.供电时,装置中的总反应为![]()
【答案】CD
【解析】
A.闭合K2制氢时,光伏电池供电,X电极与Pt电极构成电解池;闭合K1放电时,X电极与Zn电极构成原电池。据图分析,制氢时表面析出H2的Pt电极为阴极,故K+应该移向Pt电极,故A正确;
B.制氢时,X电极为电解池阳极时,Ni元素失电子、化合价升高,故电极反应式为Ni(OH)2-e-+OH-=NiOOH+H2O,故B正确;
C.供电时,发生的是原电池反应,Zn电极为负极,发生氧化反应并消耗OH-,其电极反应式为Zn-2e-+4OH-=ZnO22-+2H2O,则Zn电极附近溶液的 pH降低,故C错误;
D.供电时,X电极发生还原反应,氧化剂为NiOOH,供电时电池反应中氧化剂不是H2O,故D错误;
答案选CD。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】80 ℃时,1 L 密闭容器中充入0.20 mol N2O4,发生反应N2O4(g)2NO2(g) ΔH=Q kJ·mol-1(Q>0),获得如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
下列判断正确的是
A.升高温度该反应的平衡常数K增大
B.20~40s内,v(N2O4)=0.004mol·L-1·s-1
C.100s时再通入0.40molN2O4,达新平衡时N2O4的转化率增大
D.反应达平衡时,吸收的热量为0.15QkJ