题目内容
【题目】Na2O2是重要的化工原料,具有多种用途。
(1)写出CO2和Na2O2反应的化学方程式:___________________________________。
(2)某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗?__________,简要说明理由:_______________________________________________。
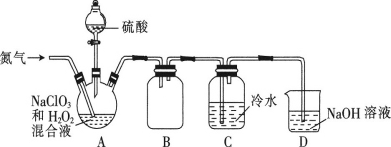
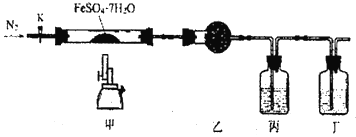
(3)该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(图中铁架台等装置已略去)。
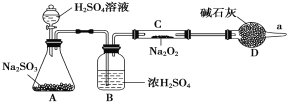
装置中B的作用是_________________,D的作用是_____________________。
(4)将足量的Na2O2投入到含有下列离子的溶液中:NO3-、S2-、HCO3-、CO32-、Na+,设反应完毕后,无固体析出,则上述离子数目减少的有__________,数目增多的离子有________。
【答案】2CO2+2Na2O2=2Na2CO3+O2 合理 由于过氧化钠具有强氧化性,能将+4价的硫氧化为+6价的硫而生成硫酸钠 干燥SO2气体,防止水蒸气进入C装置与Na2O2反应 防止空气中的水蒸气进入C装置与Na2O2反应,同时吸收过量SO2气体,便于氧气的检验和防止污染空气 S2-、HCO3- Na+、CO32-
【解析】
(1)CO2和Na2O2反应生成碳酸钠和氧气,化学方程式2CO2+2Na2O2=2Na2CO3+O2;
(2)SO2有还原性,Na2O2有强氧化性,过氧化钠能将+4价的硫氧化为+6价的硫而生成硫酸钠,所以判断合理。
(3)浓硫酸有吸水性,能吸收二氧化硫中的水分,防止水蒸气与过氧化钠反应而干扰二氧化硫;碱石灰是干燥剂,能吸收水分,防止水蒸气的干扰;碱石灰是碱性物质,能吸收二氧化硫等酸性气体,防止污染大气。
(4)Na2O2具有强氧化性,可与S2-发生氧化还原反应,则S2-数目减小,Na2O2与水反应生成NaOH可与HCO3反应,则溶液中HCO3浓度减小,CO32浓度增大,Na+的数目增多。