题目内容
【题目】某温度下,在 2L的密闭容器中,加入1molX(g)和 2molY(g)发生反应:X(g)+mY(g)3Z(g) ΔH=-Q kJ·molˉ1(Q>0),10min后该反应达到平衡时,X、Y的物质的量分别为0.9mol、1.8mol。下列叙述不正确的是
A.m=2
B.在0~10min内,X的反应速率为 0.005mol·Lˉ1·minˉ1
C.10min后,X的消耗速率等于Y的生成速率
D.在0~10min内,X和 Y反应放出的热量为 0.1Q kJ
【答案】C
【解析】
由题意建立如下三段式:

A.由变化量之比等于化学计量数之比可得0.1mol:0.2mol=1:m,解得m=2,A正确;
B. 在0~10min内,X的反应速率为![]() =0.005mol·Lˉ1·minˉ1,B正确;
=0.005mol·Lˉ1·minˉ1,B正确;
C. 10min后该反应达到平衡,由正反应速率等于逆反应速率可知,Y的生成速率是X的消耗速率的2倍,C错误;
D.设在0~10min内,X和 Y反应放出的热量为a,由X的变化量和反应热的关系可得:1mol:QkJ=0.1mol:a,解得a=0.1QkJ,D正确;
故选C。

【题目】某兴趣小组用镀锌铁皮按下列流程制备七水合硫酸锌(ZnSO4·7H2O)

相关信息如下:①金属离子形成氢氧化物沉淀的相关pH范围。
金属离子 | pH | |
开始沉淀 | 完全沉淀 | |
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Zn2+ | 5.4 | 8.2 |
②ZnSO4的溶解度(物质在100g水中溶解的质量)随温度变化曲线。
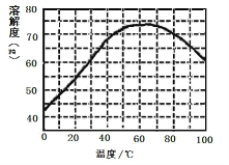
请回答:
(1)①镀锌铁皮上的油污可用Na2CO3溶液去除,理由是____________。
②步骤Ⅰ,可用于判断镀锌层完全反应的实验现象是__________________________。
(2)步骤Ⅱ,需加入过量H2O2,理由是____(请简述理由,并且写出对应的离子反应方程式)。
(3)步骤Ⅲ,合适的pH范围是____________________。
(4)步骤Ⅳ,需要用到下列所有操作:a.蒸发至溶液出现晶膜;b.在60℃蒸发溶剂;c.冷却至室温;d.在100℃蒸发溶剂;e.过滤。请给出上述操作的正确顺序_____________(操作可重复使用)。
(5)步骤Ⅴ,某同学采用不同降温方式进行冷却结晶,测得ZnSO4·7H2O晶体颗粒大小分布如下图所示。根据该实验结果,为了得到颗粒大小相对均一的较大晶粒,宜选择_______方式进行冷却结晶。

A. 快速降温 B. 缓慢降温 C. 变速降温