题目内容
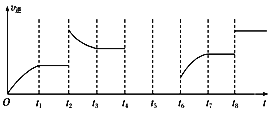
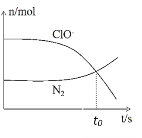
【题目】某离子反应涉及到ClO﹣、NH4+、N2、Cl﹣等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法不正确的是
A. 该反应中ClO-为氧化剂,N2为氧化产物
B. 反应后溶液的pH减小
C. 如图t0时反应达平衡状态
D. 反应过程中每生成1 mol N2,转移6mol电子
【答案】C
【解析】
通过图像,N2的物质的量增大,说明N2为生成物,ClO-的物质的量减小,说明ClO-为反应物,化学反应遵循元素守恒和原子守恒,即NH4+为反应物,Cl-为生成物,然后进行分析和判断;
通过图像,N2的物质的量增大,说明N2为生成物,ClO-的物质的量减小,说明ClO-为反应物,化学反应遵循元素守恒和原子守恒,即NH4+为反应物,Cl-为生成物,
A、根据上述分析,ClO-→Cl-,其中Cl的化合价降低,即ClO-为氧化剂,NH4+→N2,其中N的化合价升高,NH4+为还原剂,N2为氧化产物,故A说法正确;
B、该离子方程式为3ClO-+2NH4++2OH-=N2↑+5H2O+3Cl-,消耗OH-,反应后溶液的pH降低,故B说法正确;
C、根据图像t0后,物质的量仍发生变化,说明t0时没有达到平衡,故C说法错误;
D、每生成1mol N2,转移电子物质的量为1mol×2×[0-(-3)]=6mol,故D说法正确。

【题目】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知![]()
![]() kJ·mol
kJ·mol![]() )下列说法正确的是
)下列说法正确的是
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
NH3的浓度(mol·L | c1 | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 |
|
|
|
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应Ⅰ:CO(g)+2H2(g) ![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K):
温度 | 250 ℃ | 300 ℃ | 350 ℃ |
K | 2.0 | 0.27 | 0.012 |
(1)由表中数据判断ΔH1________(填“>”、“<”或“=”)0;反应CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH3=___________(用ΔH1和ΔH2表示)。
CO(g)+H2O(g) ΔH3=___________(用ΔH1和ΔH2表示)。
(2)若容器容积不变,则下列措施可提高反应Ⅰ中CO转化率的是________(填字母序号)
A.充入CO,使体系总压强增大 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.使用高效催化剂
(3)保持恒温恒容条件对于反应Ⅱ:将10 mol CO2和30mol H2放入1 L的密闭容器中,充分反应后测得CO2的转化率为60%,则该反应的平衡常数为____________________。若维持条件不变向该容器中投入10 mol CO2、30mol H2、10 mol CH3OH(g)和 10mol H2O(g),判断平衡移动的方向是________(填“正向移动”、“逆向移动”或“不移动”)。
(4)反应Ⅰ的逆反应速率与时间的关系如图所示。由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:t2时_______________________;t8时______________________________。