题目内容
4.下列事实不能用勒夏特列原理解释的是( )| A. | 光照新制的氯水时,溶液的pH逐渐减小 | |
| B. | 高温高压有利于N2和H2转化为NH3:N2(g)+3H2(g)?2NH3(g);△H<0) | |
| C. | 打开汽水瓶时,有大量气泡逸出 | |
| D. | 氨水应密闭保存于低温处 |
分析 勒夏特利原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,勒夏特利原理适用的对象应存在可逆过程,如与可逆过程的平衡移动无关,则不能用勒夏特利原理解释.
解答 解:A、氯水中存在化学平衡Cl2+H2O?HCl+HClO,光照使氯水中的次氯酸分解,次氯酸浓度减小,使得平衡向右移动,氢离子浓度变大,溶液的PH值减小,能用勒夏特列原理解释,故A不选;
B、N2(g)+3H2(g)?2NH3(g);△H<0,升高温度平衡逆向移动,不能用勒夏特列原理解释,故B选;
C、气体的溶解度随温度的升高而减小,随压强的增大而增大,由气体的溶解度随压强的增大而增大,因此常温时打开汽水瓶时,瓶内的压强减小,因此瓶内的二氧化碳会从瓶中溢出,可以用勒夏特列原理解释,故C不选;
D、氨水中存在化学平衡:NH3+H2O?NH3•H2O,平衡是放热反应温度降低,平衡向生成一水合氨的方向进行,避免氨气挥发,故D不选;
故选B.
点评 本题考查了化学平衡移动原理的分析判断,影响因素的分析,平衡移动原理的理解是解题关键,题目难度中等.

练习册系列答案
相关题目
12.对于某些常见离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钠溶液有白色沉淀产生,再加稀硝酸沉淀不消失,一定有Ag+ | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸沉淀不消失,一定有SO42- |
9.下列对溶液叙述正确的是( )
| A. | 向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小 | |
| B. | 对于物质的量浓度相同的氢氧化钠和氨水,加水稀释至m倍和n倍后,若稀释后溶液的pH相等,则m<n | |
| C. | 在中和滴定实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,须经干燥或润洗后方可使用 | |
| D. | 25℃时NH4Cl溶液的Kw大于100℃时NaCl溶液的Kw |
16.下列说法不正确的是( )
| A. | 把碳棒放在酒精喷灯上灼烧 2-3min 后即投入到冷水中,重复操作几次,可制得多孔碳棒 | |
| B. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录 溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 | |
| C. | K2CrO4 溶液中存在平衡 2CrO${\;}_{4}^{2-}$+2H+Cr2O${\;}_{7}^{2-}$+H2O,加稀硝酸则溶液由黄色变为橙色 | |
| D. | 分光光度计可以用来测定某些化学反应的反应速率 |
13.下列离子方程式书写正确的是( )
| A. | 硫酸溶液与氧氧化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| B. | 向水中通入氯气:Cl2+H2O?2H++Cl-+ClO- | |
| C. | Na与H2O反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | H${\;}_{2}^{18}$O中投入Na2O2固体:2H${\;}_{2}^{18}$O+2Na2O2═4OH-+4Na++18O2↑ |
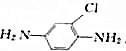 ,B与亚硝酸,在0~5℃反应后生成的产物与溴亚化铜和氰化钾反应生成C,C与氢氧化钠溶液共热生成2-氯-4-硝基苯酚,试推测A、B、C的构造式.
,B与亚硝酸,在0~5℃反应后生成的产物与溴亚化铜和氰化钾反应生成C,C与氢氧化钠溶液共热生成2-氯-4-硝基苯酚,试推测A、B、C的构造式.