题目内容
【题目】请按要求填写下列空白:
主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 | ① | ② | ③ | ④ | |||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在元素①②⑤⑥⑦⑧对应的最高价氧化物的水化物中,碱性最强的化合物的电子式是:_________________________________________;
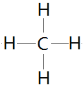
(2)写出元素②的最简单氢化物的结构式_________________________;
(3)④⑤⑥⑦四种元素的简单离子半径从大到小排序____________(用离子符号表示);
(4)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物的水化物反应的离子方程式______;
(5)写出元素③的常见氢化物和它的最高价氧化物的水化物反应的化学方程式____________。
【答案】 ![]()
 r(S2-)>r(O2-)>r(Na+)>r(Al3+)(或S2->O2->Na+>Al3+) Al2O3+2OH-=2AlO2-+H2O NH3+HNO3=NH4NO3
r(S2-)>r(O2-)>r(Na+)>r(Al3+)(或S2->O2->Na+>Al3+) Al2O3+2OH-=2AlO2-+H2O NH3+HNO3=NH4NO3
【解析】
首先根据元素在周期表中的位置判断元素名称,然后依据元素周期律以及相关物质的性质分析解答。
根据元素在周期表中的相对位置可知①~⑧分别是Li、C、N、O、Na、Al、S、Cl。则
(1)金属性越强,最高价氧化物水化物的碱性越强,在元素①②⑤⑥⑦⑧对应的最高价氧化物的水化物中,碱性最强的化合物是氢氧化钠,含有离子键和共价键,其电子式是![]() ;
;
(2)元素②的最简单氢化物是甲烷,其结构式为 ;
;
(3)核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,则④⑤⑥⑦四种元素的简单离子半径从大到小排序为r(S2-)>r(O2-)>r(Na+)>r(Al3+);
(4)元素⑥的最高价氧化物氧化铝是两性氧化物,与元素⑤的最高价氧化物的水化物氢氧化钠反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O;
(5)元素③的常见氢化物氨气和它的最高价氧化物的水化物硝酸反应的化学方程式为NH3+HNO3=NH4NO3。

【题目】在2 L密闭容器内,t℃时发生反应:N2(g)+3H2(g)![]() 2NH3(g),在体系中,n(N2)随时间的变化如下表:
2NH3(g),在体系中,n(N2)随时间的变化如下表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第5min时,N2的转化率为_______________________;
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=_____________;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为______________。(用字母填空,下同);
a.v(NH3)=0.05 mol·L-1·min-1 b.v(H2)=0.03 mol·L-1·min-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.00 l mol·L-1·s-1
(4)下列表述能作为反应达到化学平衡状态的标志是_____________。
a.反应速率v(N2):v(H2):v(NH3)=1:3:2
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2
f.v(N2)消耗=2v(NH3)消耗
g.单位时间内3mol H—H键断裂的同时2mol N—H键也断裂
【题目】碳酸钙可用作食品添加剂。以磷石膏(主要成分为CaSO4·2H2O)为原料制备碳酸钙的一种工艺流程如下:
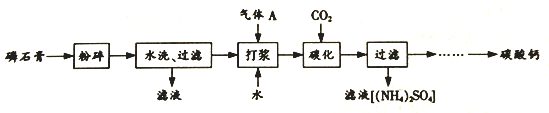
(1)已知磷石膏“水洗”前后的部分杂质质量分数变化如下表:
SiO2 | P2O5 | Al2O3 | F- | Fe2O3 | |
水洗前/% | 9.21 | 3.08 | 0.55 | 0.68 | 0.19 |
水洗后/% | 8.96 | 1.37 | 0.46 | 0.29 | 0.27 |
则“水洗“除去的主要杂质是___________。
(2)气体A的化学式为_______。
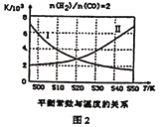
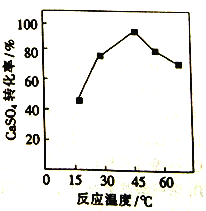
(3)“碳化”时发生反应的化学方程式为____________。其他条件一定时,“碳化”反应中CaSO4的转化率随温度的变化如右图所示,温度高于45℃,CaSO4的转化率下降的原因是________。
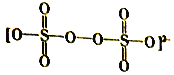
(4)工业上电解(NH4)2SO4溶液可制取过二硫酸铵[(NH4)2S2O8],其中S2O82-的结构如下。电解时阳极的电极反应式为__________,过二硫酸铵可用于游泳池中水的消毒,其原因是_________。