题目内容
【题目】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取出来的。主要步骤如下:
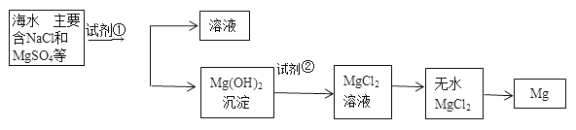
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用__________,要使MgSO4完全转化为沉淀,加入试剂①的量应________。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是_____________。
(3)试剂②可以选用____________。
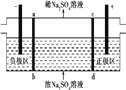
(4)无水MgCl2在熔融状态下电解,会生成Mg和Cl2,写出该反应的化学方程式:__________________。
【答案】 NaOH或石灰乳或Ca(OH)2 过量 过滤 HCl或盐酸 MgCl2(熔融)![]() Mg+Cl2↑
Mg+Cl2↑
【解析】(1)使MgSO4转化为Mg(OH)2,应选择碱,在转化中不引入新的离子,则试剂①选择NaOH或石灰乳,为了使镁离子完全转化,加入试剂①的量应过量,故答案为:NaOH或石灰乳;过量;
(2)过滤适用于不溶于水的固体和液体,分离固体和液体用过滤,所以分离得到Mg(OH)2沉淀的方法是过滤,故答案为:过滤;
(3)从氢氧化镁到氯化镁,氢氧化镁和盐酸反应得到氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O,故答案为:盐酸;
(4)氯化镁电解为分解反应,产物为镁和氯气,故答案为:MgCl2(熔融)![]() Mg+Cl2↑。
Mg+Cl2↑。

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目