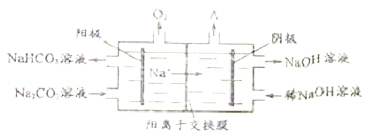
��Ŀ����
����Ŀ��ͭ����������ʹ�õĽ���֮һ������ͭ���仯�����ڹ�ҵ��������������;�dz��㷺���ش��������⣺
��1����̬+2��ͭ����M�ܲ�����Ų�ʽ��___________����4�����л�̬ԭ��δ�ɶԵ�������ͭԭ����ͬ��Ԫ����________�֡�
��2��Cu+����SCN-�γ�CuSCN��������д��һ����SCN-��Ϊ�ȵ��������_________��SCN-��Ӧ�����������ᣨH-S-CN�����������ᣨH-N=C=S�������������۵���ߵ���_______�������ƣ���ԭ����_____________________��
��3��Cu2+����NH3�γ�ƽ�������ε�[Cu(NH3)4]2+��NH3���ӵĿռ乹��Ϊ__________��[Cu(NH3)4]2+��Cu��ȡdspx�ӻ���x��ֵ��__________��
��4����֪Cu2O �۵�Ϊ1235 �棬K2O �۵�Ϊ770����ǰ���۵�ϸߣ���ԭ����___________��
��5��Cu3N �ľ������������ṹ����ͼ��ʾ��
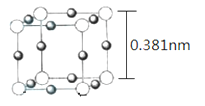
�پ������������Cu+��ľ���Ϊ________nm����������λС����
��Cu3N ������ܶ�Ϊ____________ g��cm-3����NA��ʾ����٤��������ֵ���г�����ʽ�����ؼ���������
���𰸡� 3s23p63d9 4 CO2 �� CS2 �� N2O �������� ����������Ӽ��γ���� ������ 2 ���߶������Ӿ��壬 Cu+���Ӱ뾶��K+С�������ܴ� 0.27 ![]() ��
��![]()
����������1�����������ͭ��29��Ԫ�أ����̬ԭ�ӵļ۵����Ų�ʽΪ[Ar] 3d94s1����δ�ɶԵ�����Ϊ2����̬+2��ͭ����M�ܲ㣨��3���Ӳ㣩�����Ų�ʽΪ3s23p63d9����4�����л�̬ԭ��δ�ɶԵ�������ͭԭ����ͬ��2��δ�ɶԵ��ӣ���Ԫ����Ti��Ni��Ge��Se��4�֡�
��2����SCN-��Ϊ�ȵ���������ж��֣�����3��ԭ�Ӻ�16���۵��ӣ����ݵȵ���ԭ�������ҵ�CO2��CS2��N2O �ȵ���SCN-��Ӧ�����������ᣨH-S-CN�����������ᣨH-N=C=S�������������۵���ߵ����������ᣬԭ��������������Ӽ�����γ������
��3��NH3������NΪsp3�ӻ���N��1���µ��Ӷԣ�����ռ乹��Ϊ�����Σ�[Cu(NH3)4]2+��Cu��ȡdspx�ӻ������� [Cu(NH3)4]2+�γ�ƽ�������νṹ���������ӻ������ĿΪ4�������x��ֵ��2��
��4����֪Cu2O �۵�Ϊ1235 �棬K2O �۵�Ϊ770�棬ǰ���۵�ϸߣ���ԭ���Ƕ��߶������Ӿ��壬����Cu+���Ӱ뾶��K+С����Cu2O����ľ����ܽϴ�
��5����Cu3N �ľ������������ṹʾ��ͼ��֪���þ����ı߳�Ϊ0.381nm���� Cu3N�Ļ�ѧʽ��֪���������ӵĸ�����Ϊ1:3�������а��������������![]() �����������������
�����������������![]() ����������������ӡ����������ͭ���ӡ�
����������������ӡ����������ͭ���ӡ�
����ͼ��֪���ڽ���������ͭ������һ�������ӿ����һ������ֱ�������Σ��ʾ������������Cu+��ľ���Ϊ![]() 0.27nm��
0.27nm��
��1mol Cu3N����������������ֱ�Ϊ(![]() )g��
)g��![]() �����ԣ�Cu3N ������ܶ�Ϊ
�����ԣ�Cu3N ������ܶ�Ϊ![]() g��cm-3��
g��cm-3��![]() g��cm-3��
g��cm-3��

 ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д� ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д� �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д�����Ŀ����ҵ��ˮ�г�����һ������Cr2O72-��CrO42-�����ǻ�����༰��̬ϵͳ�����ܴ���Ҫ���б�Ҫ�Ĵ�����
������������Һ�д�������ƽ�⣺2CrO42-(��ɫ)+2H+![]() Cr2O72-(��ɫ)+H2O
Cr2O72-(��ɫ)+H2O
�ֶ�ij��ҵ��ˮ���м�Ⲣ��������������ش��������⣺
(һ)ȡ���ù�ҵ��ˮ��������и��ĺ�����
�����: ȡ25.00 mL��ˮ����������ϡ�����ữ��
�����������ĵ⻯����Һ��Cr2O72-+6I-+14H+![]() 2Cr3++3I2+7H2OȻ����뼸��ָʾ���������һ�������0.1000mol��L-1 Na2S2O3��Һװ���ʽ�ζ����У����еζ��������ζ�������£���I2+2Na2S2O3
2Cr3++3I2+7H2OȻ����뼸��ָʾ���������һ�������0.1000mol��L-1 Na2S2O3��Һװ���ʽ�ζ����У����еζ��������ζ�������£���I2+2Na2S2O3![]() 2NaI+Na2S4O6��
2NaI+Na2S4O6��
�ζ����� | Na2S2O3��Һ��ʼ����/mL | Na2S2O3��Һ�յ����/mL |
��һ�� | 1.02 | 19.03 |
�ڶ��� | 2.00 | 19.99 |
������ | 0. 20 | 18.20 |
�����:��������Ӧ����Һ����pH���ڡ����˵ȴ��������ճ�������Һ������ˮ����
��1����������ϡ�����ữ��Ŀ����_____________________________��
��2�����E���жϵζ��ﵽ�յ��������___________________________��
��3�����²�������ɷ�ˮ�и������ⶨֵƫ�ߵ���_________________��
A. �ζ��յ����ʱ�����ӵζ��ܵĿ̶�
B. ʢװ����Һ����ƿ������ˮϴ����δ�ô���Һ��ϴ
C. �ζ����յ����ʱ���ֵζ��ܼ��촦����һ����Һ
D. ��ϴ��δ�ñ�Һ��ϴ��ʽ�ζ���
��4��25.00mL��ˮ���ữ����Cr2O72- �����ʵ���Ϊ___________mol.
(������ԭ��������Cr2O72-��CrO42-
�÷����Ĺ�������Ϊ��
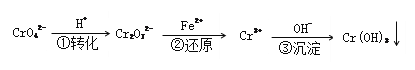
��5����˵���ڢٲ���Ӧ�ﵽƽ��״̬����_____________��������ĸ���ţ�
a. Cr2O72- ��CrO42- ��Ũ����ͬ
b. 2v(Cr2O72-)=v(CrO42-)
c. ��Һ����ɫ����
��6���ڢڲ��У���ԭ1molCr2O72-���ӣ���Ҫ________mol��FeSO4��7H2O��
��7�������£�Cr(OH)3���ܶȻ�Ksp=10-32��Ҫʹc(Cr3+)����10-5 mol��L-1����Һ��pHӦ����___________��