题目内容
5.下列物质的性质比较,正确的是( )| A. | 酸性:H2SO4>HClO4 | B. | 碱性:NaOH>KOH | ||
| C. | 非金属性:P>S | D. | 气态氢化物稳定性:HCl>H2S |
分析 A、非金属性越强,最高价氧化物的水化物酸性越强;
B、金属性越强,最高价氧化物的水化物碱性越强;
C、同周期从左到右非金属性增强;
D、非金属性越强,气态氢化物越稳定.
解答 解:A、非金属性Cl>S,最高价氧化物的水化物酸性为H2SO4<HClO4,故A错误;
B、金属性K>Na,最高价氧化物的水化物碱性为KOH>NaOH,故B错误;
C、同周期从左到右非金属性增强,所以非金属性:P<S,故C错误;
D、非金属性:Cl>S,所以气态氢化物越稳定:HCl>H2S,故D正确;
故选D.
点评 本题考查元素的性质,为高频考点,把握同主族、同周期元素的性质比较规律为解答的关键,注意元素周期律的应用和规律性知识的归纳,题目难度不大.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案
相关题目
16.下列关于有机物的叙述不正确的是( )
| A. | 石油、煤和天然气都是重要的化石燃料 | |
| B. | 淀粉、蔗糖和蛋白质均能发生水解反应 | |
| C. | 羊毛、塑料和橡胶均属于合成高分子材料 | |
| D. | 糖类、油脂和蛋白质都含有C、H、O三种元素 |
20.下列有关有机化学的说法中不正确的是( )
| A. | 按系统命名法,化合物CH3CH(CH2CH3)2名称3-甲基戊烷 | |
| B. | 用新制的Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖 | |
| C. | 有机物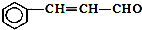 可发生加成反应、氧化反应、还原反应和聚合反应 可发生加成反应、氧化反应、还原反应和聚合反应 | |
| D. | 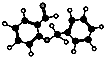 图所示的有机物分子式为C14H12O2,不能发生银镜反应 图所示的有机物分子式为C14H12O2,不能发生银镜反应 |
10.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温下,10L pH=12的Na2CO3溶液中含有的OH-离子数目为0.1NA | |
| B. | 50mL 18.4 mol/L浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA | |
| C. | 1mol羟基(-OH)中含电子数为10NA | |
| D. | 4.6g 金属钠与足量乙醇反应放出2.24L氢气 |
17.下列说法正确的是( )
| A. | 硅元素主要以单质、氧化物、硅酸盐的形式存在于自然界 | |
| B. | 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 | |
| C. | 医药中,常用酒精来消毒,是因为酒精能够使细菌蛋白质发生变性 | |
| D. | Ca(HCO3)2溶液与过量NaOH溶液反应可制得Ca(OH)2 |
15.利用金属的活泼性不同,冶炼镁、铁、汞分别应采用的方法是( )
| A. | 热还原法、热分解法、电解法 | B. | 电解法、热还原法、热分解法 | ||
| C. | 热分解法、热还原法、电解法 | D. | 电解法、热分解法、热还原法 |
 某研究性学习小组根据氧化还原反应规律,欲探究NO2、NO与Na2O2反应的情况.
某研究性学习小组根据氧化还原反应规律,欲探究NO2、NO与Na2O2反应的情况.
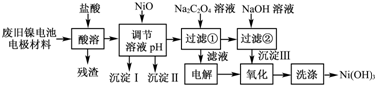
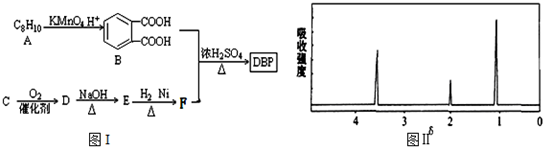
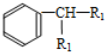 $\stackrel{KMnO_{4}.H+}{→}$
$\stackrel{KMnO_{4}.H+}{→}$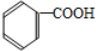
 +H2O(-R1、R2表示氢原子或烃基)
+H2O(-R1、R2表示氢原子或烃基) ,反应类型为取代反应
,反应类型为取代反应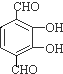 、
、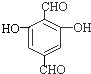 等.
等.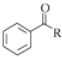 $→_{(S)-CBS}^{邻苯二酚硼烷}$
$→_{(S)-CBS}^{邻苯二酚硼烷}$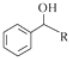 .根据已有知识并结合相关信息,写出以
.根据已有知识并结合相关信息,写出以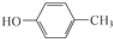 和CH3COOH为原料制备
和CH3COOH为原料制备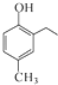 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.