题目内容
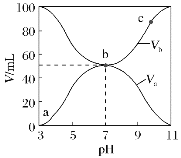
【题目】25℃时,将浓度均为0.1mol·L-1、体积分别为Va和Vb的HX溶液与NH3·H2O溶液不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法正确的是( )
A.Ka(HX)的值与Kb(NH3·H2O)的值相等
B.b点,c(NH4+)+c(HX)=0.05mol·L-1
C.a→c点过程中,一定有c(NH4+)>c(X-)>c(H+)>c(OH-)
D.a、b、c三点,c点时水电离出的c(H+)最大
【答案】AB
【解析】
根据图式可知,酸溶液的pH=3,则c(H+)<0.1mol/L,说明HA是弱酸;碱溶液的pH=11,c(OH)<0.1mol/L,则NH3H2O是弱碱;
A.酸碱恰好完全反应时溶液的pH=7,溶液呈中性,说明HA电离程度和NH3H2O电离程度相同,则Ka(HX)的值与Kb(NH3H2O)的值相等,故A正确;
B.b点,溶液显中性,HX和NH3·H2O的初始浓度为0.1mol·L-1,等体积混合后, c(H+)=c(OH),电荷守恒为c(OH)+c(X-)=c(NH4+)+c(H+),则c(NH4+)=c(X-),HX溶液的物料守恒为:c(X-)+c(HX)=0.05mol·L-1,故c(NH4+)+c(HX)=0.05mol·L-1,故B正确;
C.a→c点过程中,随着氨水的加入,溶液的由酸性变为中性,再变为碱性,c点时,c(H+)<c(OH-) ,故C错误;
D.a、b、c三点,c点显碱性,a点显酸性,对水的电离都有抑制作用,b点的溶液显中性,没有抑制水的电离,故b点时水电离出的c(H+)最大,故D错误;
答案选AB。

 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】锰酸锂(LiMn2O4)可作为锂离子电池的正极材料,在工业上可利用软锰矿浆(主要成分为MnO2,含少量Fe2O3、FeO、Al2O3、SiO2等杂质)吸收含硫烟气(主要成分SO2)制备锰酸锂,生产流程如下:
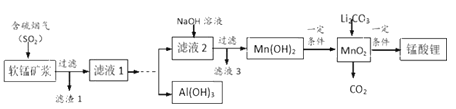
已知:①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强。②在此流程中部分金属阳离子生成氢氧化物沉淀的pH如下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)为提高含硫烟气中SO2的吸收率,可以采取的措施_____________(举一例)。
(2)滤液1中所含金属阳离子有Mn2+、_____________(填离子符号)。
(3)在实际生产中,Li2CO3与MnO2按物质的量之比1∶4混合均匀加热制取LiMn2O4,反应过程如下:
①升温到515℃时,Li2CO3开始分解产生CO2,同时生成固体A,此时比预计Li2CO3的分解温度(723℃)低得多,可能原因是_________________;
②升温到566℃时,MnO2开始分解产生另一种气体X,X恰好与①中产生的CO2物质的量相等,同时得到固体B。请写出此过程反应的化学方程式___________;
③升温到720℃时,第三阶段反应开始,固体质量逐渐增加,当质量不再增加时,得到高纯度的锰酸锂。请写出该阶段反应的化学方程式_________________。
(4)请补充完整由“滤液1”得到“滤液2”同时回收Al(OH)3的实验方案[Al(OH)3在pH≥12时溶解]:边搅拌边向滤液1中________________。(实验中须用到的试剂有:NaOH溶液、H2O2、CO2)