题目内容
1.NA表示阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 1mol Fe与足量氧气反应时转移的电子数为2NA | |
| B. | 2L 0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1mol Na2O2固体中含离子总数为4NA | |
| D. | 丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA |
分析 A.铁与氧气反应生成四氧化三铁,产物中铁元素的化合价为+$\frac{8}{3}$价;
B.2L 0.5mol•L-1硫酸钾溶液中含有溶质硫酸钾1mol,1mol硫酸钾中带有2mol负电荷;
C.1mol过氧化钠固体中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子;
D.丙烯和环丙烷的最简式都是CH2,根据最简式计算出混合物中含有氢原子数目.
解答 解:A.铁与氧气反应生成四氧化三铁,四氧化三铁中铁元素的化合价为+$\frac{8}{3}$价,则1mol铁完全反应失去$\frac{8}{3}$mol电子,转移的电子数为$\frac{8}{3}$NA,故A错误;
B.2L 0.5mol•L-1硫酸钾溶液中含有溶质硫酸钾的物质的量为1mol,1mol硫酸钾中带有2mol负电荷,阴离子所带电荷数约为2NA,故B错误;
C.1mol Na2O2固体中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子,含离子总数为3NA,故C错误;
D.42g丙烯和环丙烷的混合物中含有42g最简式CH2,含有最简式的物质的量为:$\frac{42g}{14g/mol}$=3mol,含有氢原子的物质的量为额6mol,含有的氢原子的个数为6NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
11.下列食品添加剂与类别对应正确的一组是( )
| A. | 着色剂--胡萝卜素、苯甲酸钠 | |
| B. | 调味剂--亚硝酸钠、味精 | |
| C. | 防腐剂--日落黄、山梨酸钾 | |
| D. | 营养强化剂--酱油中加铁、粮食制品中加赖氨酸 |
12.在高温条件下,利用CO与铁矿石反应冶炼金属铁的方法属于( )
| A. | 热分解法 | B. | 热还原法 | C. | 电解法 | D. | 置换法 |
9.下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
| A. | NH4CO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O↑+CO2↑ | B. | 2Na2O2+2 H2O═4NaOH+O2↑ | ||
| C. | H2O+Cl2?HCl+HClO | D. | NH3+SO2+H2O═NH4HSO3 |
6.下列实验操作及其离子方程式的评价合理的是( )
| 选项 | 实验操作及其离子方程式 | 评价 |
| A | 少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | 正确 |
| B | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓ | 错误.溴乙烷不能电离出Br- |
| C | Ca(HCO3)2溶液与等物质的量NaOH溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O | 错误.Ca2+与HCO3-的物质的量之比为1:2 |
| D | 氢氧化钡溶液与等物质的量的稀硫酸混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O | 正确 |
| A. | A | B. | B | C. | C | D. | D |

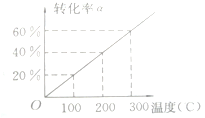 已知反应:X(g)+2Y(g)?2Z(g),将X和Y气体按体积比1:2混合于一密闭容器中,并加压到3×107Pa时达到平衡状态,此时反应物、生成物的物质的量之比为6:1,则如右图所示,此时反应对应的温度为( )
已知反应:X(g)+2Y(g)?2Z(g),将X和Y气体按体积比1:2混合于一密闭容器中,并加压到3×107Pa时达到平衡状态,此时反应物、生成物的物质的量之比为6:1,则如右图所示,此时反应对应的温度为( )