题目内容
2.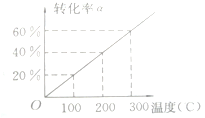 已知反应:X(g)+2Y(g)?2Z(g),将X和Y气体按体积比1:2混合于一密闭容器中,并加压到3×107Pa时达到平衡状态,此时反应物、生成物的物质的量之比为6:1,则如右图所示,此时反应对应的温度为( )
已知反应:X(g)+2Y(g)?2Z(g),将X和Y气体按体积比1:2混合于一密闭容器中,并加压到3×107Pa时达到平衡状态,此时反应物、生成物的物质的量之比为6:1,则如右图所示,此时反应对应的温度为( )| A. | 100℃ | B. | 200℃ | C. | 300℃ | D. | 400℃ |
分析 设出X、Y的物质的量,根据“平衡状态时反应物、生成物的物质的量之比为6:1”利用化学平衡三段式列式计算出反应消耗的Y的物质的量,再计算出Y的转化率,最后根据图象判断反应温度即可.
解答 解:假设X和Y物质的量分别为1mol、2mol,达平衡时消耗Y物质的量为x,则:
X+2Y?2Z
起始量(mol) 1 2 0
变化量(mol) 0.5x x x
平衡量(mol) 1-0.5x 2-x x
平衡后,测得混合气体中反应物的总物质的量与成物的总物质的量之比为6:1,则
(1-0.5x+2-x):x=6:1,
解得:x=0.4mol,
Y的转化率=$\frac{0.4mol}{2mol}$×100%=20%,
结合图象可知,该反应温度为100℃,
故选A.
点评 本题考查了化学平衡的计算,题目难度中等,明确化学平衡的含义为解答关键,注意掌握化学平衡三段式在计算中的应用方法,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1mol Fe与足量氧气反应时转移的电子数为2NA | |
| B. | 2L 0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1mol Na2O2固体中含离子总数为4NA | |
| D. | 丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA |
10.下列说法不正确的是( )
| A. | 仅含有碳、氢元素的有机物叫烃 | B. | 甲烷是最简单的有机物 | ||
| C. | 乙烷、丙烷均不存在同分异构体 | D. | 含碳元素的物质都是有机物 |
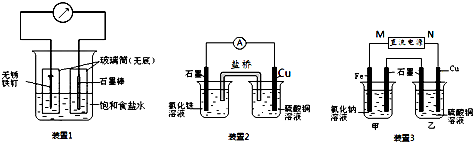
17. 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )
 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )| A. | x是正极,y是负极,CuSO4溶液的pH逐渐减小 | |
| B. | x是正极,y是负极,CuSO4溶液的pH保持不变 | |
| C. | x是负极,y是正极,CuSO4溶液的pH 逐渐减小 | |
| D. | x是负极,y是正极,CuSO4溶液的pH保持不变 |
7.蓄电池在放电时起原电池的作用,在充电时起电解池的作用,下式是爱迪生蓄电池分别在充电和放电时发生的反应:Fe+NiO2+2H2O $?_{充电}^{放电}$Fe(OH)2+Ni(OH)2
下列有关对爱迪生蓄电池的推断错误的是( )
下列有关对爱迪生蓄电池的推断错误的是( )
| A. | 放电时,Fe作负极,发生氧化反应 | |
| B. | 放电时,NiO2作正极,发生还原反应 | |
| C. | 蓄电池的电极应浸入碱性电解质溶液中 | |
| D. | 充电时,充电机的正极接在该蓄电池的负极 |
14.下列说法正确的是( )
| A. | 化学反应不一定有分子碰撞 | B. | 发生有效碰撞的分子是活化分子 | ||
| C. | 具有较高能量的分子是活化分子 | D. | 化学反应的活化能一定大于零 |