题目内容
16.(1)25g CuSO4•5H2O蓝色晶体中,CuSO40.1mol,H2O0.5mol,Cu2+0.1mol,SO42-0.1mol,O0.9mol;(2)19.6g H2SO4分子中有:①1.4NA个原子;②12.8g氧原子.
分析 (1)根据n=$\frac{m}{M}$计算出硫酸铜晶体的物质的量,再根据硫酸铜晶体计算出水、铜离子、硫酸根离子和氧原子的物质的量,关系为:n(CuSO4•5H2O)=n(CuSO4)=$\frac{1}{5}$n(H2O)=$\frac{1}{9}$n(O),由此分析解答;
(2)根据n=$\frac{m}{M}$计算出硫酸的物质的量,然后根据1mol硫酸中含有7mol的原子,4mol的氧原子,再结合m=nM计算.
解答 解:(1)25gCuSO4•5H2O的物质的量为:n(CuSO4•5H2O)=$\frac{25g}{250g/mol}$=0.1mol,0.1mol CuSO4•5H2O中CuSO4物质的量为0.1mol,含有结晶水的物质的量为:0.1mol×5=0.5mol;0.1mol CuSO4•5H2O中含Cu2+ 0.1mol;0.1mol CuSO4•5H2O中含SO42- 0.1mol0.1mol CuSO4•5H2O中含有氧原子的物质的量为:0.1mol×(4+5)=0.9mol,
故答案为:0.1;0.5;0.1;0.1;0.9;
(2)硫酸的物质的量为:$\frac{19.6g}{98g/mol}$=0.2mol,所以原子数为0.2×7×NA=1.4NA,氧原子的物质的量为:0.2mol×4=0.8mol,所以质量为:0.8mol×16g/mol=12.8g,故答案为:1.4NA;12.8.
点评 本题综合考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意相关计算公式的运用,难度不大.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
6.下列有关0.2mol•L-1 BaCl2溶液的说法中,不正确的是( )
| A. | 500 mL溶液中Ba2+和Cl-总数为0.3NA | |
| B. | 500 mL溶液中Ba2+浓度为0.2 mol•L-1 | |
| C. | 500 mL溶液中Cl-总数为0.2 NA | |
| D. | 500 mL溶液中Cl-浓度为0.2 mol•L-1 |
1.NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1mol Fe与足量氧气反应时转移的电子数为2NA | |
| B. | 2L 0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1mol Na2O2固体中含离子总数为4NA | |
| D. | 丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA |
17. 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )
 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则下列说法正确的是( )| A. | x是正极,y是负极,CuSO4溶液的pH逐渐减小 | |
| B. | x是正极,y是负极,CuSO4溶液的pH保持不变 | |
| C. | x是负极,y是正极,CuSO4溶液的pH 逐渐减小 | |
| D. | x是负极,y是正极,CuSO4溶液的pH保持不变 |
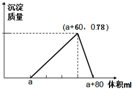
 把1.71克硫酸铝配成100ml溶液,为了抑制水解,在配置过程中加入少量硫酸.若在上述溶液中逐滴加入0.5mol/L的氢氧化钠溶液,直至过量.用图象记录滴加过程中产生沉淀的过程.
把1.71克硫酸铝配成100ml溶液,为了抑制水解,在配置过程中加入少量硫酸.若在上述溶液中逐滴加入0.5mol/L的氢氧化钠溶液,直至过量.用图象记录滴加过程中产生沉淀的过程.