题目内容
【题目】某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为( )

A. 1∶1∶4
B. 1∶3∶1
C. 3∶3∶8
D. 1∶1∶1
【答案】A
【解析】试题分析:氧化性强弱顺序:HNO3>Fe3+>Cu2+,0~1时发生Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,消耗1molFe的同时消耗4mol硝酸,生成1molFe3+,1~2时发生Fe+2Fe3+=3Fe2+,消耗1molFe同时消耗2molFe3+,因此原溶液中Fe3+的物质的量为1mol,2~3时发生Fe+Cu2+=Fe2++Cu,消耗1molFe的同时消耗1molCu2+,则原溶液中有1 molCu2+,溶液的体积相同,浓度之比等于物质的量之比为:1:1:4,故选项A正确。

【题目】某地环保部门将收集到的一定量酸雨试样分成甲、乙、丙、丁四份,进行如图所示的实验探究。
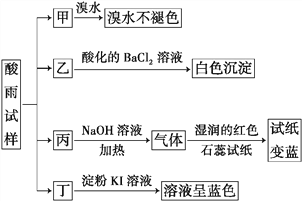
已知酸雨试样中可能含有下表所示的某些离子:
阳离子 | Na+、Mg2+、X |
阴离子 | Cl-、SO32-、Y、NO3- |
请回答下列问题:
(1)X是________________________,Y是__________________________。
(2)可能存在的阴离子是______________________,能证明该阴离子是否存在的简单实验操作为_______________________________________________________________________________________________________________________。
(3)写出丁试样中滴加淀粉KI溶液所发生反应的离子方程式: ______________________________________。