题目内容
2.短周期元素W、X、Y和Z的原子序数依次增大.元素W的一种核素不含中子,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍.下列说法错误的是( )| A. | 元素W、X的氯化物中,各原子均满足最外层8电子的稳定结构 | |
| B. | 元素X与W形成的原子数比为1:1的化合物有很多种,且都存在非极性键 | |
| C. | 非金属性:Z>X | |
| D. | 元素Z可与元素Y形成化合物Y2Z3,该化合物易水解 |
分析 短周期元素W、X、Y和Z的原子序数依次增大.元素W在所有元素中原子半径最小,则W为H元素;X原子的最外层电子数是内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,则X为C元素;元素Y是地壳中含量最丰富的金属元素,则Y为Al;Z原子的最外层电子数是其电子层数的2倍,原子序数大于Al,位于第三周期,故最外层电子数为6,则Z为S元素,结合元素化合物的结构性质解答.
解答 解:短周期元素W、X、Y和Z的原子序数依次增大.元素W在所有元素中原子半径最小,则W为H元素;X原子的最外层电子数是内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,则X为C元素;元素Y是地壳中含量最丰富的金属元素,则Y为Al;Z原子的最外层电子数是其电子层数的2倍,原子序数大于Al,位于第三周期,故最外层电子数为6,则Z为S元素,
A.W为H元素,HCl中H原子最外层电子数为2,故A错误;
B.X为C元素,对应的氢化物为烃,比值为1:1的化合物有乙炔、苯等,含有碳碳键,为非极性键,故B正确;
C.Z为Al,X为H,非金属性H较强,形成AlH3的化合物,故C错误;
D.Al2S3在水溶液中发生水解反应生成氢氧化铝与硫化氢,故D正确.
故选AC.
点评 本题考查原子结构与元素性质知识,侧重于物质结构与性质等方面的考查,难度不大,注意原子核外电子的排布特点,推断元素的种类为解答该题的关键.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
13.下列各组物质性质的排列顺序的不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | B. | 碱性:KOH>NaOH>Mg(OH)2 | ||
| C. | 熔沸点:HI>HBr>HCl>HF | D. | 稳定性:HF>H2O>H2S |
17.下列各实验装置图的叙述中,正确的是( )
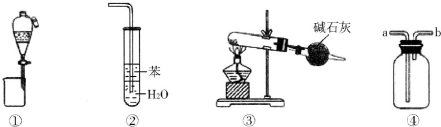

| A. | 装置①可用于分离苯和溴苯的混合物 | |
| B. | 装置②可用于吸收氨气,且能够防止倒吸 | |
| C. | 以NH4Cl为原料,装置③可用于制备NH3 | |
| D. | 剩用装置④可收集Cl2、H2等气体,盛满水时还能收集NO等气体 |
7.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3- | |
| B. | 常温下,c(H+)/c(OH-)=1010的溶液中:Na+、NH4+、ClO-、I- | |
| C. | 水电离出的c(H+)=10-12mol•L-1的溶液:K+、Na+、CO32-、Br- | |
| D. | 含有0.1mol•LHCO3-的溶液:Na+、Fe3+、NO3-、SCN- |
14.下列图示与对应的叙述一定正确的是( )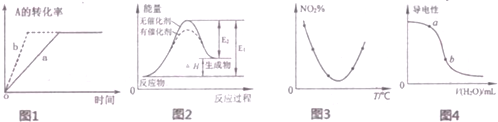

| A. | 图1所示反应:A(g)+2B(g)?3C(g),b曲线表示的一定是增大压强 | |
| B. | 图2表示催化剂能改变化学反应的焓变 | |
| C. | 图3表示等量N02在容积相同的恒容密闭容器中,不同温度下分别发生反应;2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 | |
| D. | 图4表示向稀CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
11.下列变化中属于原电池反应的是( )
| A. | 在空气中金属铝表面迅速氧化形成保护层 | |
| B. | 钢铁在潮湿的空气中生锈 | |
| C. | 红热的铁丝与冷水接触,表面形成蓝黑色保护层 | |
| D. | 钢管被原油中的含硫化合物腐蚀 |
12.甲烷与氧气的反应式放热反应,下列对应的图象正确的是( )
| A. |  | B. | 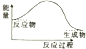 | C. | 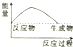 | D. |  |