题目内容
16.(A)下列有机实验操作或叙述,正确的是④⑤(填写代号).①能使酸性高锰酸钾溶液褪色的烃,分子中一定含有碳碳双键或者碳碳叁键
②乙酸乙酯中含有少量乙酸可用饱和的Na0H溶液除去
③蔗糖水解时应用浓H2SO4作催化剂
④在鸡蛋清溶液中滴入饱和的NH4NO3溶液后有沉淀析出
⑤银镜反应的实质是Ag+把-CHO氧化成-COOH
⑥实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸
(B)25℃~101kPa时,mg仅含三种元素的有机物在足量的O2中充分燃烧.其燃烧产物通入过量的Na2O2固体,固体质量增加了mg.
①下列物质中不能满足上述结果的是CD
A.C2H6O2 B.C6H12O6 C.C12H22O11 D.(C6H10O5)n
②A是符合上述条件且相对分子质量最小的有机物,则A的电子式
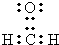 .A中所有原子是否共面是(填“是”或“否”).
.A中所有原子是否共面是(填“是”或“否”).(C)用系统命名法命名下列物质:
①
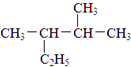 :2,3-二甲基戊烷;②
:2,3-二甲基戊烷;②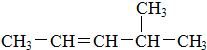 :4-甲基-2-戊烯.
:4-甲基-2-戊烯.
分析 (A)①苯的同系物如甲苯能使酸性高锰酸钾溶液褪色;
②乙酸乙酯在NaOH溶液中水解;
③浓H2SO4具有脱水性;
④鸡蛋清溶液中滴入饱和的NH4NO3溶液,发生盐析;
⑤-CHO能被弱氧化剂氧化;
⑥应先加入浓硝酸,最后加入浓硫酸.
(B)有机物燃烧,H元素转化为H2O,C元素转化为CO2,燃烧产物与Na2O2反应:2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2=2Na2CO3+O2,由反应方程式可知,过氧化钠增加的质量即为H2、CO的质量,故mg只含C、H、O三种元素的有机物在足量氧气中充分燃烧,其燃烧产物立即与过量的过氧化钠反应,固体质量增加mg,因此有机物化学组成符合(CO)m•(H2)n满足题意,
①根据分析可知,有机物分子中C、O原子数相等即可;
②满足条件的有机物为甲醛,甲醛为共价化合物,其分子中存在1个碳氧双键和2个碳氢键,据此写出其电子式;根据甲醛中C原子的杂化方式进行判断其构型.;
(C)判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:
(1)烷烃命名原则:
①长:选最长碳链为主链;
②多:遇等长碳链时,支链最多为主链;
③近:离支链最近一端编号;
④小:支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简:两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面;
(2)有机物的名称书写要规范;
(3)对于结构中含有苯环的,命名时可以依次编号命名,也可以根据其相对位置,用“邻”、“间”、“对”进行命名;
(4)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小.
解答 解:(A)①苯的同系物如甲苯能使酸性高锰酸钾溶液褪色,则不一定含双键或三键,故错误;
②乙酸乙酯在NaOH溶液中水解,不能除杂,应选饱和碳酸钠溶液除杂,故错误;
③浓H2SO4具有脱水性,使蔗糖碳化,应选稀硫酸作催化剂,故错误;
④鸡蛋清溶液中滴入饱和的NH4NO3溶液,发生盐析,则有沉淀析出,故正确;
⑤-CHO能被弱氧化剂氧化,则银镜反应的实质是Ag+把-CHO氧化成-COOH,故正确;
⑥为防止酸液的飞溅,应先加入浓硝酸,最后加入浓硫酸,故错误;
故答案为:④⑤;
(B)有机物燃烧,H元素转化为H2O,C元素转化为CO2,燃烧产物与Na2O2反应:2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2=2Na2CO3+O2,由反应方程式可知,过氧化钠增加的质量即为H2、CO的质量,故mg只含C、H、O三种元素的有机物在足量氧气中充分燃烧,其燃烧产物立即与过量的过氧化钠反应,固体质量增加mg,因此有机物化学组成符合(CO)m•(H2)n满足题意,
①根据分析可知,有机物化学组成符合(CO)m•(H2)n,则其分子中C、O原子数必须相同,满足条件的为A、B,不满足条件的为C、D,
故答案为:CD;
②有机物化学组成符合(CO)m•(H2)n,且相对分子质量最小的有机物A为:HCHO,其电子式为: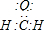 ;甲醛分子中含有碳氧双键,中心原子C原子以sp2杂化轨道成键,甲醛中不存在未成键电子对,则甲醛分子为平面结构,则其分子中所有原子共平面,
;甲醛分子中含有碳氧双键,中心原子C原子以sp2杂化轨道成键,甲醛中不存在未成键电子对,则甲醛分子为平面结构,则其分子中所有原子共平面,
故答案为: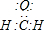 ;是;
;是;
(C)①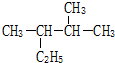 是烷烃,选取最长碳原子的为主链,主链含有5个,从离甲基最近的一端编号,该有机物名称为:2,3-二甲基戊烷,
是烷烃,选取最长碳原子的为主链,主链含有5个,从离甲基最近的一端编号,该有机物名称为:2,3-二甲基戊烷,
故答案为:2,3-二甲基戊烷;
②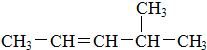 :从离双键最近的一端编号,该有机物命名为:4-甲基-2-戊烯,故答案为:4-甲基-2-戊烯.
:从离双键最近的一端编号,该有机物命名为:4-甲基-2-戊烯,故答案为:4-甲基-2-戊烯.
点评 本题考查化学实验方案的设计,为高频考点,涉及有机物的结构与性质、有机物的制备及混合物分离提纯、有机物分子式确定的计算、命名等,把握性质及实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

 名校课堂系列答案
名校课堂系列答案| A. | Na,Al,Fe | B. | Zn,Cu,Al | C. | Ca,Na,K | D. | Zn、Ca,Al |
| A. | Al3+ NH4+ SO42-Cl- | B. | Na+Mg2+ HCO3- NO3- | ||
| C. | K+ Na+ AlO2-Cl- | D. | Fe2+ K+NO3-Cl- |
| A. | .c(Na+)=c(HB-)+2c(B2-)+c(OH-) | B. | .c(Na+)=0.1mol•L-1≥c(B2-) | ||
| C. | .c(H+)•c(OH-)=10-14 | D. | 此溶液的pH=1 |
 下列①②对应的试剂(或条件)不能完成实验目的是( )
下列①②对应的试剂(或条件)不能完成实验目的是( )| 实验目的 | 试剂(或条件) | |
| A | 温度对H2O2分解反应速率的影响 | ①热水浴②冰水浴 |
| B | 用稀硫酸比较铝和铁的金属活动性 | ①铝粉 ②铁钉 |
| C | 用酸化的AgNO3溶液检验海水中Cl-能否蒸馏除去 | ①海水 ②蒸馏所得液体 |
| D | 用Na块检验乙醇分子存在不同于烃分子里的氢原子 | ①乙醇 ②煤油 |
| A. | A | B. | B | C. | C | D. | D |
| A. | SO2 | B. | H2O | C. | Na2O | D. | CaSiO |
 硼(B)及其化合物在化学中有重要的地位.请回答下列问题:
硼(B)及其化合物在化学中有重要的地位.请回答下列问题: 向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题: