题目内容
【题目】已知N、P同属于元素周期表的第ⅤA族元素,N在第二周期,P在第三周期。![]() 分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是
分子呈三角锥形,N原子位于锥顶,3个H原子位于锥底,N—H键间的夹角是![]() 。
。
(1)![]() 分子的空间结构为
分子的空间结构为![]() ,它是一种_____(填“极性”或“非极性”)分子。
,它是一种_____(填“极性”或“非极性”)分子。
(2)![]() 分子与
分子与![]() 分子的构型关系_____(填“相同”“相似”或“不相似”),P—H键_____(填“有”或“无”)极性,
分子的构型关系_____(填“相同”“相似”或“不相似”),P—H键_____(填“有”或“无”)极性,![]() 分子_______(填“有”或“无”)极性。
分子_______(填“有”或“无”)极性。
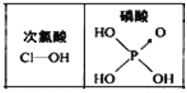
(3)![]() 是一种淡黄色油状液体,下列对
是一种淡黄色油状液体,下列对![]() 的有关描述不正确的是___(填字母)。
的有关描述不正确的是___(填字母)。
a.该分子呈平面三角形
b.该分子中的化学键为极性键
c.该分子为极性分子
d.因N—Cl键的键能大,故![]() 稳定
稳定
【答案】非极性 相似 有 有 a
【解析】
(1) ![]() 分子的空间结构为
分子的空间结构为![]() ,为正四面体,所有键角键长均相等,分子里电荷分布是对称的(正负电荷中心能重合),是一种非极性分子,故答案为:非极性;
,为正四面体,所有键角键长均相等,分子里电荷分布是对称的(正负电荷中心能重合),是一种非极性分子,故答案为:非极性;
(2) N原子与P原子结构相似,NH3分子与PH3分子的结构也相似,NH3分子与PH3分子中心原子孤对电子数均=![]() =1,价层电子对数=3,杂化轨道数=3+1,N、P原子为sp3杂化,有一对孤电子占据空轨道,所以分子构型均为三角锥形,正负电荷中心不重合,所以NH3分子与PH3分子均有极性,不同原子之间形成的共价键是极性键,故答案为:相似;有;有;
=1,价层电子对数=3,杂化轨道数=3+1,N、P原子为sp3杂化,有一对孤电子占据空轨道,所以分子构型均为三角锥形,正负电荷中心不重合,所以NH3分子与PH3分子均有极性,不同原子之间形成的共价键是极性键,故答案为:相似;有;有;
(3) a.NCl3有一对孤电子,价层电子对数=3+1=4,为sp3杂化,加之有一对孤电子占据轨道,所以NCl3呈三角锥形,a错误;
b.不同种原子之间形成的共价键为极性键,b正确;
c.该分子为极性键构成的极性分子,c正确;
d.键能越大,分子越稳定,因N—Cl键的键能大,故NCl3稳定,d正确;
故答案为:a。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案【题目】I.常温下,HNO2电离反应的平衡常数值为2.6×10-4。NaNO2是一种重要的食品添加剂,由于其外观及味道都与食盐非常相似,误食工业用盐造成食物中毒的事件时有发生。
(1)某活动小组同学设计实验方案鉴别 NaCl溶液和NaNO2溶液,请填写下列表格。
选用药品 | 实验现象 | 利用NaNO2的性质 |
①酚酞试液 | ____________ | ____________ |
②淀粉-KI试纸 | ____________ | ____________ |
(2)亚硝酸钠有毒,不能随意排放,实验室一般将其与饱和氯化铵溶液共热使之转化成无毒无公害的物质,其产物之一为无色无味气体,则该气体为____________(填化学式)。
II.活动小组同学采用如下装置制备并测定所得固体中亚硝酸钠(NaNO2)的质量分数(装置可重复使用,部分夹持仪器已省略)。
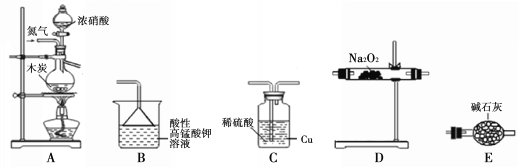
已知: ①2NO + Na2O2 =2NaNO2;
②酸性条件下,NO、NO2都能与MnO4-反应生成NO3-和Mn2+;NaNO2能使
酸性高锰酸钾溶液褪色。
(1)实验装置的连接顺序为____________;
(2)C瓶内发生反应的离子方程式为____________。
(3)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10 mol·L-1的酸性KMnO4溶液进行滴定,实验所得数据如下表。
滴定次数 | 1 | 2 | 3 | 4 |
KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
①第一组实验数据出现较明显异常,造成异常的原因可能是__________(填字母序号)。
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶用蒸馏水洗净后未干燥
c.观察滴定终点时仰视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为____________。
(4)设计实验,比较0.1mol·L-1NaNO2溶液中NO2-的水解程度和0.1mol·L-1HNO2溶液中HNO2电离程度的相对大小_______(简要说明实验步骤、现象和结论,仪器和药品自选)。