题目内容
3.化学实验装置的正确连接是实验成败的关键,如图是中学化学中常见的实验装置.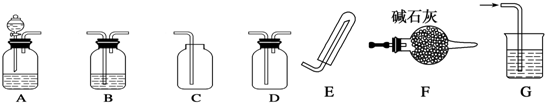
(1)用上述装置制备气体:
①要快速制取并得到干燥的NH3,正确的仪器组合是AFE(按制气装置顺序填仪器的编号字母),制气所选用的固体药品是固体氢氧化钠或氧化钙.
②若用H2O2和MnO2来制取和收集干燥的O2,则应选择的正确仪器组合是ABC (按制气装置顺序填仪器的编号字母),检验气体收集满的方法是将带火星的木条靠近集气瓶口,若木条复燃,则说明氧气收集满了.
(2)甲同学用A、B组合来验证盐酸、碳酸、次氯酸的酸性强弱时,则盐酸应装入分液漏斗(填仪器名称)中,B装置中发生反应的离子方程式为Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO.
分析 (1)①固体氢氧化钠和浓氨水可以快速制取氨气;
②氧气的密度比空气大;氧气能使带火星的木条复燃;
(2)用强酸制弱酸原理解题.
解答 解:(1)①利用固体氢氧化钠和浓氨水可以快速制取氨气.氨气密度比空气小,所以采用向下排空气法收集,
故答案为:AFE;固体氢氧化钠或氧化钙;
②氧气的密度比空气大,所以采用向上排空气法收集,正确的组合为ABC,检验O2收集满的方法是将带火星的木条靠近集气瓶口,若木条复燃,则说明氧气收集满了,
故答案为:ABC;将带火星的木条靠近集气瓶口,若木条复燃,则说明氧气收集满了;
(2)在利用A、B组合验证盐酸、碳酸、次氯酸的酸性强弱时,可以采用强酸制弱酸的方法,A中利用盐酸和碳酸钠反应制取二氧化碳,盐酸应装入分液漏斗,将二氧化碳通入B中的次氯酸钙中,可反应生成次氯酸和CaCO3 沉淀,反应方程式:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO,
故答案为:分液漏斗;Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO.
点评 本题考查化学实验方案设计,根据气体制备原理、收集和检验方法解题,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化最小的是( )
| A. | 水 | B. | 盐酸 | C. | 醋酸溶液 | D. | NaCl溶液 |
11.下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为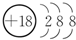 .
.
(2)表中能形成两性氢氧化物的元素是铝(填元素名称),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O═2KAlO2+3H2↑.
(3)①、④、⑤、⑥、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为KOH、Mg(OH)2、Al(OH)3、H2CO3、H2SO4、HClO4(用化学式表示).
(4)③元素与⑩元素两者核电荷数之差是26.
(5)请写出②的氢化物发生催化氧化的化学方程式4NH3+5O2催化剂_△4NO+6H2O.
(6)请写出⑤元素的最高价氧化物的水化物与⑦元素的最高价氧化物的水化物反应的离子方程式Al(OH)3+3H+═Al3++3H2O.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
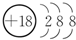 .
.(2)表中能形成两性氢氧化物的元素是铝(填元素名称),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O═2KAlO2+3H2↑.
(3)①、④、⑤、⑥、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为KOH、Mg(OH)2、Al(OH)3、H2CO3、H2SO4、HClO4(用化学式表示).
(4)③元素与⑩元素两者核电荷数之差是26.
(5)请写出②的氢化物发生催化氧化的化学方程式4NH3+5O2催化剂_△4NO+6H2O.
(6)请写出⑤元素的最高价氧化物的水化物与⑦元素的最高价氧化物的水化物反应的离子方程式Al(OH)3+3H+═Al3++3H2O.
8.有X、Y、Z、W 四种含14个电子的粒子,其结构特点如下:
(1)A 原子核外比 X 原子多3个电子,A 的原子结构示意图是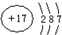 ,含1mol X 的氧化物晶体中含有共价键数目为4NA或2.408×1024
,含1mol X 的氧化物晶体中含有共价键数目为4NA或2.408×1024
(2)Z与钙离子组成的化合物的电子式为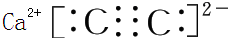
(3)28g Y 完全燃烧放出的热量是283.0kJ,写出 Y 燃烧的热化学方程式2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ/mol
(4)组成W的元素最高价氧化物对应的水化物甲有如图所示转化关系(反应条件和其他物质已略)甲丁→乙丁→丙
①写出丁在高温下与水反应的化学方程式3Fe+4H2O高温_Fe3O4+4H2或C+H2O(g)高温_CO+H2
②组成W的元素的简单氢化物极易溶于水的主要原因是NH3与H2O间能形成氢键,该氢化物与空气可以构成一种燃料电池,电解质溶液是KOH,其负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
| 粒子代码 | X | Y | Z | W |
| 原子核数 | 单核 | 不同元素构成的两核 | 同元素构成的两核 | 同元素构成的两核 |
| 粒子的电荷数 | 0 | 0 | 两个负电荷 | 0 |
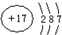 ,含1mol X 的氧化物晶体中含有共价键数目为4NA或2.408×1024
,含1mol X 的氧化物晶体中含有共价键数目为4NA或2.408×1024(2)Z与钙离子组成的化合物的电子式为
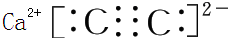
(3)28g Y 完全燃烧放出的热量是283.0kJ,写出 Y 燃烧的热化学方程式2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ/mol
(4)组成W的元素最高价氧化物对应的水化物甲有如图所示转化关系(反应条件和其他物质已略)甲丁→乙丁→丙
①写出丁在高温下与水反应的化学方程式3Fe+4H2O高温_Fe3O4+4H2或C+H2O(g)高温_CO+H2
②组成W的元素的简单氢化物极易溶于水的主要原因是NH3与H2O间能形成氢键,该氢化物与空气可以构成一种燃料电池,电解质溶液是KOH,其负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
12.若M+N=F+G这一反应是放热反应,下列说法正确的是( )
| A. | M的能量比G高 | |
| B. | N的能量比G高 | |
| C. | 这一反应不需要加热一定能发生 | |
| D. | 反应物的能量之和大于生成物的能量之和 |
13.以石墨为电极,电解1L CuSO4和NaCl的混合溶液,其中CuSO4与NaCl的物质的量之和为0.2mol,CuSO4的物质的量占总物质的量的比值为a.下列说法正确的是( )
| A. | 若a=0.5,当Cu2+在阴极恰好全部析出时,产生的气体只有氯气 | |
| B. | 若a=0.5,当Cu2+在阴极恰好全部析出时,产生的气体的物质的量为0.1mol | |
| C. | 若a=0.2,当Cl-在阳极恰好全部逸出时,产生0.08mol的NaOH | |
| D. | 若电解一段时间后,阴、阳两极产生的气体的物质的量恰好均为0.16mol,则a=0.2 |
 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知: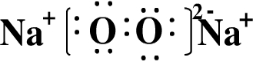 ,含有的化学键类型为离子键和共价键,Z2Y2为离子晶体.
,含有的化学键类型为离子键和共价键,Z2Y2为离子晶体.