题目内容
【题目】X、Y、Z、W为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断正确的是( )
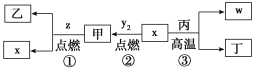
A.反应①、②属于氧化还原反应,③属于非氧化还原反应
B.Y的离子半径比Z的离子半径小
C.反应③可以证明X的非金属性强于W
D.一定条件下,x与甲反应生成丁
【答案】D
【解析】
根据题中信息可判断x为碳,丙为二氧化硅,在高温条件下碳与二氧化硅反应生成w为硅、丁为一氧化碳;y2为氧气,碳与氧气点燃反应生成甲为二氧化碳,z为镁,二氧化碳在镁中点燃反应生成碳和乙为氧化镁。
A. 反应①为镁和二氧化碳反应,反应过程镁和碳元素化合价均发生变化,是氧化还原反应,反应②为碳在氧气中点燃,是氧化还原反应,反应③为碳和二氧化硅反应,反应过程中碳和硅元素化合价均发生变化,是氧化还原反应,故A项错误;
B.Y的离子为O2-,Z的离子为Na+,电子层数均为两层,但氧离子的核电荷小于钠离子,故氧离子半径大于钠离子,故B项错误;
C.根据元素周期律,非金属性越强,单质氧化性越强,反应③为:![]() ,反应中C将Si元素还原,不能说明C的非金属性强于Si,故C项错误;
,反应中C将Si元素还原,不能说明C的非金属性强于Si,故C项错误;
D.碳可以和二氧化碳在高温条件下反应生成一氧化碳,故D项正确;
故答案为D。

【题目】![]() 年,比利时人索尔维
年,比利时人索尔维![]()
![]() 用氨碱法生产碳酸钠.反应原理如下:
用氨碱法生产碳酸钠.反应原理如下:

![]() 时一些物质在水中的溶解度
时一些物质在水中的溶解度![]()
NaCl |
|
|
|
|
|
|
|
|
|

(1)氨碱法生成纯碱的原料是____________,可循环利用的物质有____________.
(2)饱和NaCl溶液通![]() 和
和![]() 能生成
能生成![]() 的原因有:____________/span>.
的原因有:____________/span>.
Ⅲ![]() 我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(3)生产中需向分离出![]() 后所得的溶液中加入NaCl固体并通入
后所得的溶液中加入NaCl固体并通入![]() ,在____________
,在____________![]() 填温度范围
填温度范围![]() 下析出____________
下析出____________![]() 填化学式
填化学式![]()
【题目】下列实验操作、实验现象和实验结论均正确的是( )
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 将Al2(SO4)3溶液和NaHCO3溶液混合 | 产生白色沉淀,并有大量气体生成 | 生成Al2(CO3)3沉淀和CO2气体 |
B | 在淀粉溶液中加入几滴稀硫酸,水浴5min,加入NaOH溶液调溶液pH至碱性,再加入新制的Cu(OH)2悬浊液,加热 | 有红色沉淀生成 | 淀粉完全水解 |
C | 将少量SO2气体通过足量Na2O2 | 余下气体能使带火星木条复燃 | 有O2生成 |
D | 用pH试纸分别测定等浓度的A、B两溶液(可能为NaHCO3或者Na2CO3)的pH值 | pHA> pHB | A溶液为Na2CO3溶液 |
A. A B. B C. C D. D