题目内容
(15分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:

现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
(1)称量样品所用的仪器为_____(填“托盘天平”或“电子天平”),将样品研细后再反应,其目的是_______ 。
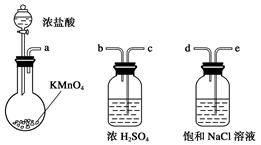
(2)装置a和c的作用分别是____和____(填标号)。
A除去SO2气体 B除去空气中的水蒸气 C有利于气体混合
D有利于观察空气流速 E除去反应后多余的氧气
(3)上述反应结束后,仍需通一段时间的空气,其目的是___________。
(4)通过计算可知,该黄铜矿的纯度为________。
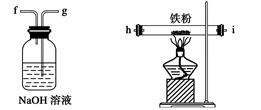
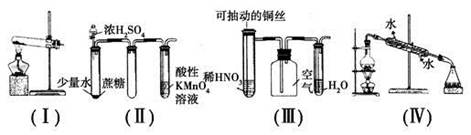
(5)若用右图装置替代上述实验装置d,同样可以达到实验目的的是____(填序号)。

(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有_____________________________________________。

现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的
 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:(1)称量样品所用的仪器为_____(填“托盘天平”或“电子天平”),将样品研细后再反应,其目的是_______ 。
(2)装置a和c的作用分别是____和____(填标号)。
A除去SO2气体 B除去空气中的水蒸气 C有利于气体混合
D有利于观察空气流速 E除去反应后多余的氧气
(3)上述反应结束后,仍需通一段时间的空气,其目的是___________。
(4)通过计算可知,该黄铜矿的纯度为________。
(5)若用右图装置替代上述实验装置d,同样可以达到实验目的的是____(填序号)。

(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有_____________________________________________。
(1)电子天平,使原料充分反应、加快反应速率。 (2)B、D和E
(3)使反应生成的SO2全部进入d装置中,使结果精确。(4)80%;(5)②;
(6) 空气中的CO2与Ba(OH)2反应生成BaCO3沉淀;BaSO3被氧化成BaSO4
(3)使反应生成的SO2全部进入d装置中,使结果精确。(4)80%;(5)②;
(6) 空气中的CO2与Ba(OH)2反应生成BaCO3沉淀;BaSO3被氧化成BaSO4
试题分析:(1)由于托盘天平的准确度为0.1g,但是要称量的质量是1.150g。因此称量样品所用的仪器为电子天平;将样品研细后再反应,其目的是增大接触面积,使原料充分反应、加快反应速率。(2)装置a的作用是除去空气中的水蒸气;混合气体,有利于观察空气流速,因此选项为BD;装置c的作用除去反应后多余的氧气。选项为E。(3)上述反应结束后,仍需通一段时间的空气,其目的是使反应生成的SO2全部进入d装置中,使结果精确。(4)SO2与碘水反应的方程式是I2+SO2+2H2O=H2SO4+2HI。根据元素守恒可得CuFeS2~2SO2~2I2,n(I2)= 0.05mol/L×0.02L×10=0.01mol.所以n(CuFeS2)=0.005mol;m(CuFeS2)= 0.005mol×184g/mol=0.92g,所以该黄铜矿的纯度为(0.92g÷1.150g)×100%=80%。(5)①与SO2不能发生反应,不能吸收。错误,②能够吸收SO2的装置。正确。③是用来测量气体体积的,不能用来吸收气体。错误。(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有空气中的CO2与Ba(OH)2反应生成BaCO3沉淀;BaSO3被氧化成BaSO4。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


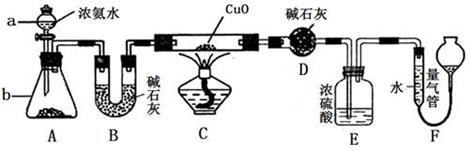
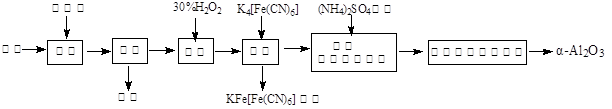
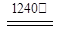 2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过图9所示的装置。
2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过图9所示的装置。



 3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH