题目内容
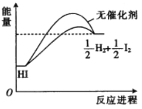
【题目】在有、无催化剂时,HI分解反应的能量随反应进程的变化关系如图所示,下列说法正确的是
A.其他条件不变时,升高温度,平衡体系中HI的含量降低
B.图示中无催化剂的反应焓变更高
C.其他条件不变时,增大压强,可提高HI的平衡转化率
D.催化剂可提高分子的能量,加快反应速率
【答案】A
【解析】
由图示可知,HI(g)![]()
![]() I2(g)+
I2(g)+![]() H2(g)是吸热反应;
H2(g)是吸热反应;
A.HI(g)![]()
![]() I2(g)+
I2(g)+![]() H2(g)是吸热反应,升高温度平衡正向移动,平衡体系中HI的含量降低,故A正确;
H2(g)是吸热反应,升高温度平衡正向移动,平衡体系中HI的含量降低,故A正确;
B.催化剂能改变反应活化能,但不改变反应热效应,即有无催化剂,反应焓变△H均不变,故B错误;
C.对HI(g)![]()
![]() I2(g)+
I2(g)+![]() H2(g)反应达到平衡后,增大压强,平衡不移动,不能提高HI的转化率,故C错误;
H2(g)反应达到平衡后,增大压强,平衡不移动,不能提高HI的转化率,故C错误;
D.催化剂可降低反应的活化能,增大活化分子百分数,加快反应速率,故D错误;
故答案为A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】下表中依据热化学方程式得到的对应结论正确的是
热化学方程式 | 结论 | |
A | 稀溶液中:H+(aq)+OH-(aq)=H2O (l) △H=-57.3kJ.mol-1 | 将稀硫酸与氢氧化钡溶液混合后,若有1molH2O 生成,则放出的能量为57.3kJ |
B | Sn(s,灰) | 锡制品在炎热的夏天更容易损坏 |
C | P4(s,白磷)=4P(s,红磷) △H=-29.2kJ.mol-1 | 常温下红磷比白磷更稳定 |
D | C3H8(g)+5O2(g)=3CO2 (g)+4H2O(g) △H=-2043.9kJ.mol-1 | C3H8的燃烧热△H=-2043.9kJ.mol-1 |
A.AB.BC.CD.D



