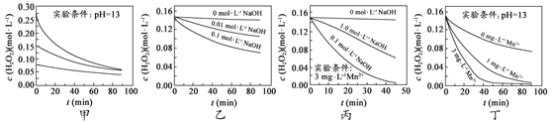
题目内容
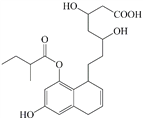
【题目】某物质只含C. H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表化学键:单键、双键等)。
(1)该物质的结构简式为_________;
(2)该物质中所含官能团的名称为_________、_________;
(3)下列物质中,与该产品互为同分异构体的是______(填序号);与该产品互为同系物的是(填序号)________;
①CH3CH═CHCOOH ②CH2═CHCOOCH3 ③CH3CH2CH═CHCOOH ④CH3CH(CH3)COOH.
(4)下列对该物质性质的说法中,不正确的是_________。
A.它能使酸性高锰酸钾褪色 B.它能发生加成反应 C.它能发生酯化反应 D.它能发生水解反应
【答案】![]() 碳碳双键 羧基 ①② ③ D
碳碳双键 羧基 ①② ③ D
【解析】
某物质只含C、 H、O三种元素,其分子模型为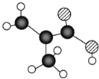 ,则
,则![]() 代表碳原子、
代表碳原子、![]() 代表氧原子、
代表氧原子、![]() 代表氢原子。按碳形成4个共价键,氧形成2个共价键,氢形成1个共价键的原则,可确定原子间形成的共价键为单键还是双键。
代表氢原子。按碳形成4个共价键,氧形成2个共价键,氢形成1个共价键的原则,可确定原子间形成的共价键为单键还是双键。
(1)由以上分析,可确定该物质的结构简式为![]() 。答案为:
。答案为:![]() ;
;
(2)该物质中所含官能团的名称为碳碳双键、羧基。答案为:碳碳双键;羧基;
(3) ![]() 与CH3CH═CHCOOH和CH2═CHCOOCH3分子式都为C4H6O2,但结构不同,三者互为同分异构体,故选①②;
与CH3CH═CHCOOH和CH2═CHCOOCH3分子式都为C4H6O2,但结构不同,三者互为同分异构体,故选①②;![]() 与CH3CH2CH═CHCOOH都为烯酸,官能团的种类和数目都相同,且分子组成上相差1个“CH2”,二者互为同系物,故选③。答案为:①②;③;
与CH3CH2CH═CHCOOH都为烯酸,官能团的种类和数目都相同,且分子组成上相差1个“CH2”,二者互为同系物,故选③。答案为:①②;③;
(4) A.![]() 分子中含有碳碳双键,能使酸性高锰酸钾褪色,A不合题意;
分子中含有碳碳双键,能使酸性高锰酸钾褪色,A不合题意;
B.![]() 分子中含有碳碳双键,能发生加成反应,B不合题意;
分子中含有碳碳双键,能发生加成反应,B不合题意;
C.![]() 分子中含有羧基,能发生酯化反应,C不合题意;
分子中含有羧基,能发生酯化反应,C不合题意;
D.![]() 不能发生水解反应,D符合题意;
不能发生水解反应,D符合题意;
故选D。答案为:D。