题目内容
【题目】实验发现,298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是( )

A. 该原电池的正极反应是Zn-2e-==Zn2+
B. 该电池总反应为3Zn+2Fe3+==2Fe+3Zn2+
C. 该电池铂电极上有气泡出现
D. 左烧杯中溶液的血红色逐渐褪去
【答案】D
【解析】A、该原电池的负极反应是Zn-2e-=Zn2+,正极反应是Fe3++e-=Fe2+,选项A错误;B、该电池总反应为Zn+2Fe3+=2Fe2++Zn2+,选项B错误;C、铂电极上的反应为Fe3++e-=Fe2+,电极上没有气泡出现,选项C错误;D、左烧杯中反应为Fe3++e-=Fe2+,溶液的血红色逐渐褪去,选项D正确。答案选D。

【题目】某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。
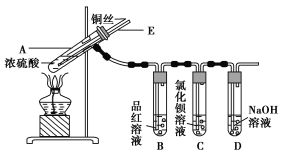
实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为 。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是 。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 |
写出其中SO2表现还原性的离子反应方程式: 。
(4)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是 。
(5)实验完毕后,装置中残留的气体有毒,不能打开导管上的胶塞。为了防止该气体排入空气中污染环境,拆除装置前,应当采取的操作是 。
(6)将SO2气体通入含有n mol Na2S的溶液中,充分反应后,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体 mol(不考虑溶解的SO2)。