题目内容
【题目】现有下列4种物质:①Na2O2、②SiO2、③SO2、④NaHCO3固体。其中,
(1)与水反应,生成能使带火星木条复燃的固体是________(填序号);
(2)能使品红溶液褪色且加热时又复原的是_________(填序号);
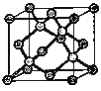
(3)上述物质中有1种物质难溶于水,该物质在一定条件下与焦炭发生反应,可制得电脑芯片以及太阳能电池的材料,该反应的化学方程式为:_______________________________;
(4)上述物质中有1种物质可以用来除去多余的胃酸,它还是常见的疏松剂,主要是因为它在加热条件下产生了气体,使食品变疏松。写出其受热分解的化学方程式___________。
【答案】 ① ③ SiO2 + 2C ![]() Si + 2CO ↑ 2NaHCO3
Si + 2CO ↑ 2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
【解析】(1)Na2O2与水反应生成NaOH和氧气,能使带火星木条复燃,故答案为:①;
(2)二氧化硫具有漂白性,能使品红溶液褪色且加热时又复原,故答案为:②;
(3)SiO2难溶于水,一定条件下与焦炭发生反应生成硅和一氧化碳,反应的化学方程式为SiO2 + 2C ![]() Si + 2CO ↑,故答案为:SiO2 + 2C
Si + 2CO ↑,故答案为:SiO2 + 2C ![]() Si + 2CO ↑;
Si + 2CO ↑;
(4)NaHCO3不稳定,加热易分解,生成碳酸钠和二氧化碳、水,碳酸氢钠能够与酸反应,用来除去多余的胃酸。碳酸氢钠受热分解的化学方程式为2NaHCO3![]() Na2CO3+H2O+CO2↑,故答案为:2NaHCO3
Na2CO3+H2O+CO2↑,故答案为:2NaHCO3![]() Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目