题目内容
【题目】下列各组物质中,能用酸性高锰酸钾溶液鉴别的是( )
A. 乙烯、乙炔
B. 己烷、苯
C. 己烯、苯
D. 苯、甲苯
【答案】CD
【解析】能用高锰酸钾酸性溶液鉴别的有机物可能含有不饱和键、苯的同系物或醛,以此解答该题。
乙烯和乙炔都含有不饱和键,都能与酸性高锰酸钾发生氧化还原反应,不能鉴别,A错误;苯、己烷与酸性高锰酸钾都不反应,不能鉴别,B错误;己烯含有碳碳双键,可与酸性高锰酸钾反应,苯与酸性高锰酸钾不反应,可鉴别,C正确;甲苯能与酸性高锰酸钾发生氧化还原反应,使其褪色,苯与酸性高锰酸钾不反应,现象不同,能鉴别,D正确;正确选项CD。

【题目】(1)用0.lmol·L-1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol·L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
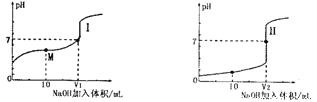
①滴定醋酸的曲线是__________(填“I”或“Ⅱ”)。
②V1和V2的关系:V1______V2(填“>”、“=”或“<”)
③M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是_______________。
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。资料:AgSCN是白色沉淀
操作步骤 | 现象 |
步骤1:向2mL0.005mol·L-1AgNO3溶液中 加入2mL0.005mol·L-1KSCN溶液,静置 | 出现白色沉淀 |
步骤2:取lmL上层清液于试管中,滴加1 滴2 mol·L-1Fe(NO3)3溶液 | 溶液变红色 |
步骤3:向步骤2的溶液中,继续加入5滴3mol·L-1 AgNO3溶液 | 出现白色沉淀,溶液红色变浅 |
步骤4:向步骤1余下的浊液中加入5滴3 mol·L-1 KI溶液 | 出现黄色沉淀 |
①写出步骤2中溶液变红色的离子方程式______________________。
②用化学平衡原理解释步骤3的实验现象______________________。