题目内容
【题目】按要求完成下列问题:
(1)分离胶体和溶液常用的方法叫______________。
(2)除去KNO3溶液中少量杂质AgNO3,可选择加入___________溶液,然后过滤。
(3)已知下列六种物质:熔融KI 、Cl2 、CaCO3固体 、食盐晶体、石墨 、盐酸 ,能导电的电解质是_______________。
(4)100克质量分数46%的酒精(C2H6O)水溶液中含氧原子_________NA。
(5)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是_________。
【答案】渗析 适量KCl 熔融KI 4 22.4bc/(aNA)L
【解析】
(1) 胶体的分散质粒子直径为1-100nm, 溶液中粒子的直径小于1nm,胶体的粒子不能透过半透膜,溶液中粒子可以透过半透膜,所以可以用渗析的方法把胶体和溶液分离开;答案:渗析。
(2)除去KNO3溶液中少量杂质AgNO3,可选择加入适量的KCl溶液,然后过滤即可;答案:适量KCl。
(3)电解质是在水溶液或熔融状态下能导电的化合物,如熔融KI、CaCO3固体 、食盐晶体属于电解质,能导电的是:熔融KI。答案:熔融KI。
(4)100克含酒精质量分数46%的溶液中含有乙醇的质量为:m(C2H6O)=100g![]() 46g,乙醇中含氧原子数N=46g /46g
46g,乙醇中含氧原子数N=46g /46g![]() mol-1
mol-1![]() NA=NA;水的质量m=100g-46g=54g, 水中含氧原子数N=54g/18g
NA=NA;水的质量m=100g-46g=54g, 水中含氧原子数N=54g/18g![]() mol-1
mol-1![]() NA=3NA;所以100克质量分数46%的酒精(C2H6O)水溶液中含氧原子NA +3NA =4NA。答案:4
NA=3NA;所以100克质量分数46%的酒精(C2H6O)水溶液中含氧原子NA +3NA =4NA。答案:4
(5)因为ag某气体中含有的分子数为b,所以a/M=b/NA,M=aNA/b,则cg该气的物质的量=c/M=bc/aNA mol,在标准状况下的体积是22.4![]() bc/(aNA)=22.4bc/(aNA)L,答案:22.4bc/(aNA)。
bc/(aNA)=22.4bc/(aNA)L,答案:22.4bc/(aNA)。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案【题目】用如图所示装置进行气体x的性质实验,得出的实验结论正确的是
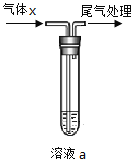
选项 | 实验操作 | 实验现象 | 实验结论 | |
制备气体x | 溶液a | |||
A | 乙醇与浓硫酸共热至170℃ | KMnO4酸性溶液 | 紫色褪去 | C2H4被氧化 |
B | 碳酸钠与醋酸溶液作用 | Na2SiO3溶液 | 产生白色沉淀 | H2CO3的酸性强于H2SiO3 |
C | 双氧水与二氧化锰作用 | KI淀粉溶液 | 溶液变蓝 | O2能将I-氧化为I2 |
D | 溴乙烷与氢氧化钠醇溶液共热 | Br2的四氯化碳溶液 | 橙红色褪去 | C2H4与Br2发生加成反应 |
A. A B. B C. C D. D