题目内容
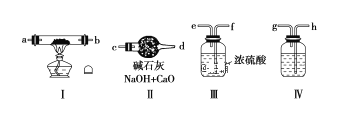
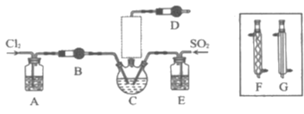
【题目】随着5G时代的到来,半导体材料将迎来快速发展,三氯化氧磷(POCl3)常用作半导体掺杂剂及光导纤维原料。一研究小组在实验室利用PCl3、SO2、Cl2在60~65°C时反应制备POCl3和SOCl3的实验装置如图所示(气体的制备装置未画出)。
资料卡片:
物质 | 熔点/°C | 沸点/°C | 其他 |
PCl3 | -93.6 | 76.1 | 遇水剧烈水解,易与O2反应 |
POCl3 | 1.25 | 105.8 | 遇水剧烈水解,能溶于PCl3 |
SOCl3 | -105 | 78.8 | 遇水剧烈水解,受热易分解 |
(1)该反应的化学方程式为___。
(2)A、B装置中的试剂分别是___、___。
(3)装置E的作用是___。
(4)反应装置的虚线框中未画出的仪器最好选用___(填“F”或“G”),理由是___。
(5)反应结束后,提纯POCl3的操作是___(填操作名称)。
(6)测定某掺杂剂中POCl3的含量(杂质不参与反应):准确称取4.000g样品在水解瓶中摇动至完全水解,将水解液配成250mL溶液,取25.00mL于锥形瓶中,加入0.4000molL-1的AgNO3溶液25.00mL,再加少许硝基苯,用力振荡。加入NH4Fe(SO4)2作指示剂,用0.l000molL-1KSCN标准溶液滴定过量的AgNO3至终点,消耗KSCN标准溶液22.00mL。[已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12,Ag3PO4可溶于硝酸,POCl3的相对分子质量为153.5]
①加入少量的硝基苯的目的是___。
②POCl3的质量分数为___。(保留一位小数)
【答案】PCl3+SO2+Cl2![]() POCl3+SOCl2 饱和食盐水 P2O5或无水CaCl2 干燥SO2,通过观察产生气泡的速率控制通入气体的流速 F 球形冷凝管接触面积大,便于反应中各物质冷凝回流 蒸馏 覆盖在AgCl表面,避免AgCl转化为AgSCN 99.8%
POCl3+SOCl2 饱和食盐水 P2O5或无水CaCl2 干燥SO2,通过观察产生气泡的速率控制通入气体的流速 F 球形冷凝管接触面积大,便于反应中各物质冷凝回流 蒸馏 覆盖在AgCl表面,避免AgCl转化为AgSCN 99.8%
【解析】
本题考查PCl3、SO2、Cl2在60~65°C时反应制备POCl3和SOCl3的实验,根据资料卡片,本实验必须在无水条件下反应,所以装置A用饱和食盐水除去氯气中的氯化氢,B用P2O5或无水CaCl2除去氯气中的水蒸气,E用浓硫酸除去二氧化硫中的水蒸气,且A和E都可以通过观察产生气泡的速率控制通入气体的流速,D用无水CaCl2防止空气中的水蒸气进入,用F球形冷凝管进行冷凝回流,将PCl3充分反应,提高产率。
(1)该反应在60~65°C时反应,化学方程式为:PCl3+SO2+Cl2![]() POCl3+SOCl2;
POCl3+SOCl2;
(2)A装置用饱和食盐水除去氯气中的氯化氢,B装置用P2O5或无水CaCl2除去氯气中的水蒸气,所以A、B装置中的试剂分别是饱和食盐水、P2O5或无水CaCl2;
(3)装置E用浓硫酸除去二氧化硫中的水蒸气,且控制产生气泡的速率控制反应速率,所以E的作用是干燥SO2,通过观察产生气泡的速率控制通入气体的流速;
(4)球形冷凝管与直球形冷凝管最大区别是球形冷凝管接触面积大,冷凝效果更好,能将反应物和生成物都充分冷凝回流,增加产率,所以虚线框中用球形冷凝管F,因为球形冷凝管接触面积大,便于反应中各物质冷凝回流;
(5)根据资料卡片POCl3和SOCl2的沸点不同,所以提纯POCl3的操作是蒸馏;
(6)①根据Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12,AgSCN溶解度更小,所以用KSCN标准溶液滴定过量的AgNO3时,要避免AgCl转化为AgSCN,影响测定,故加入少量的硝基苯的目的是覆盖在AgCl表面,避免AgCl转化为AgSCN ;
②根据条件可知:AgNO3的总物质的量为:0.4mol/L×0.025L=0.01mol, KSCN的物质的量为0.1mol/L×0.022L=0.0022mol,SCN-反应的Ag+为0.0022mol,Cl-反应的Ag+为0.01mol- 0.0022mol=0.0078 mol,Cl-的物质的量是0.0078 mol,根据元素守恒则25ml中POCl3物质的量是0.0078 mol×![]() =0.0026 mol,则4.000g样品中POCl3物质的量是0.0026 mol×10=0.026 mol,POCl3的质量分数为
=0.0026 mol,则4.000g样品中POCl3物质的量是0.0026 mol×10=0.026 mol,POCl3的质量分数为![]() =99.8%。
=99.8%。