题目内容
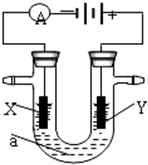
18.电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则①电解池中X极上的电极反应式为2H++2e-=H2↑.
在X极附近观察到的实验现象是酚酞变红,有气泡产生.②Y电极上的电极反应式为2Cl--2e-=Cl2↑.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是粗铜,电极反应式为Cu-2e-=Cu2+.
②Y电极的材料是纯铜,电极反应式为Cu2++2e-=Cu.(说明:杂质发生的电极反应不必写出)电解一段时间后,CuSO4溶液的浓度将变小(填“变大”、“变小”或“不
 变”)
变”)
分析 (1)若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极上氯离子放电生成氯气,X电极上氢离子放电,同时该电极附近生成氢氧根离子;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阴极上铜离子放电;
解答 解:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极上氯离子放电生成氯气,电极反应式为2Cl--2e-=Cl2↑,
和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,故答案为:2H++2e-=H2↑;酚酞变红,有气泡产生;2Cl--2e-=Cl2↑;
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,阳极应该是粗铜、阴极是纯铜,则X电极是纯铜、Y电极是粗铜,阳极发生反应为:Cu-2e-=Cu2+,阴极上铜离子放电,电极反应式为Cu2++2e-=Cu,电解一段时间后,因为阳极先是比铜活泼的金属失电子,但阴极一直未铜离子得电子,所以CuSO4溶液的浓度将变小;
故答案为:粗铜; Cu-2e-=Cu2+;纯铜;Cu2++2e-=Cu;变小.
点评 本题考查原电池原理,为高频考点,侧重于学生的分析能力的考查,本题涉及电极反应式的书写、检验等知识点,知道离子放电顺序及电极反应式的书写方法,题目难度不大.

练习册系列答案
相关题目
8.咖啡鞣酸具有较广泛的抗菌作用,结构简式如图所示:关于咖啡鞣酸的下列叙述不正确的是( )
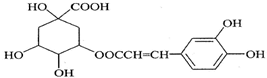
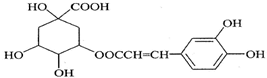
| A. | 分子式为C16H18O9 | |
| B. | 1 mol咖啡鞣酸水解时可消耗8molNaOH | |
| C. | 与苯环上碳直接相连的原子都在同一平面上 | |
| D. | 与浓溴水既能发生取代反应又能发生加成反应 |
6.恒容密闭容器中进行的可逆反应2NO2?2NO+O2,不能说明达到平衡状态的是( )
| A. | 单位时间内生成a mo1 O2的同时生成2a mol NO2 | |
| B. | 单位时间内生成a mol O2的同时生成2a mol NO | |
| C. | 混合气体的颜色不再改变 | |
| D. | 混合气体的压强不再改变 |
3.NA代表阿伏加德常数,下列说法正确的是( )
| A. | 0.1mol/L Na2CO3溶液中含有0.2molNa+ | |
| B. | 在常温常压下,11.2L氮气所含的原子数目为NA | |
| C. | 2g氢气所含原子数目为NA | |
| D. | 在常温常压下,18 g水中含有的分子数为NA |
7.下列离子方程式书写正确的是( )
| A. | 稀硫酸滴到铁片上:Fe+H+═Fe2++H2↑ | |
| B. | 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-═Cu(OH)2↓ | |
| C. | 碳酸钠溶液与稀盐酸反应:CO32-+2H+═H2CO3 | |
| D. | 碳酸氢钠溶液与盐酸混合:HCO3-+H+═H2O+CO2↑ |
8.下列化学用语表达正确的是( )
| A. | 硫原子的结构示意图: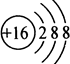 | |
| B. | 氨气(NH3)中氮元素的化合价:+3 | |
| C. | 氧化铁的化学式:FeO | |
| D. | 碳酸氢钠电离方程式:NaHCO3═Na++HCO3- |
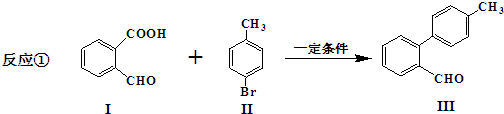
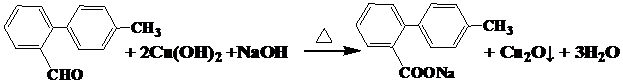 .
.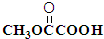 与
与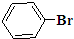 也可以发生类似反应①的反应,有机产物的结构简式为:
也可以发生类似反应①的反应,有机产物的结构简式为: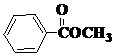 .
.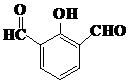 、
、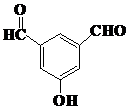 、
、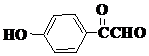 (任意两种).(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)
(任意两种).(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种) ;取代反应;
;取代反应; ;取代反应;
;取代反应; ;加聚反应;
;加聚反应; CH3CH2OOCCOOCH2CH3+2H2O;酯化反应;
CH3CH2OOCCOOCH2CH3+2H2O;酯化反应;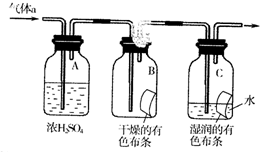 氯气是一种化学性质活泼的非金属单质,工业上
氯气是一种化学性质活泼的非金属单质,工业上