题目内容
3.NA代表阿伏加德常数,下列说法正确的是( )| A. | 0.1mol/L Na2CO3溶液中含有0.2molNa+ | |
| B. | 在常温常压下,11.2L氮气所含的原子数目为NA | |
| C. | 2g氢气所含原子数目为NA | |
| D. | 在常温常压下,18 g水中含有的分子数为NA |
分析 A.缺少溶液体积,无法计算溶液中钠离子的数目;
B.常温常压下,不能使用标况下的气体摩尔体积计算;
C.氢气的摩尔质量为2g/mol,氢气分子中含有2个氢原子;
D.根据n=$\frac{m}{M}$计算出18g水的物质的量,再计算出含有分子数.
解答 解:A.没有告诉碳酸钠溶液的体积,无法计算溶液中钠离子的数目,故A错误;
B.不是标准状况下,不能使用标况下的气体摩尔体积计算11.2L氮气的物质的量,故B错误;
C.2g氢气的物质的量为:$\frac{2g}{2g/mol}$=1mol,1mol氢气分子中含有2molH原子,所含原子数目为2NA,故C错误;
D.18g水的物质的量为:$\frac{18g}{18g/mol}$=1mol,含有的分子数为NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的综合应用,题目难度中等,注意明确标况下气体摩尔体积的使用条件,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系;A为易错点,注意题中缺少溶液体积.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
14.下列实验基本操作(或实验注意事项)中,主要是出于实验安全考虑的是( )
| A. | 可燃性气体的验纯 | |
| B. | 实验剩余的药品不能放回原试剂瓶 | |
| C. | 滴管不能交叉使用 | |
| D. | 气体实验装置在实验前进行气密性检查 |
11.中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示.下列叙述正确的是( )
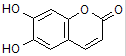

| A. | M的相对分子质量是180 | |
| B. | 1 mol M最多能与2 mol Br2发生反应 | |
| C. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1 mol M与足量NaHCO3反应能生成2 mol CO2 |
8.检验在空气中露置一段时间的FeSO4溶液中是否含有Fe3+,可选用的试剂是( )
| A. | KSCN溶液 | B. | BaCl2溶液 | C. | 酸性KMnO4溶液 | D. | 盐酸 |
15.有下列两个反应.当温度降低时.反应a平衡右移.反应b平衡左移.
a、C2H2(g)+H2(g)?C2H4(g)
b、2CH4(g)?C2H4(g)+2H2(g)
报据上述变化.判断以下几个热化学方程式:
①C(s)+2H2(g)?CH4(g)△H=-Q1 kJ•mol-1
②2C(s)+H2(g)?C2H2(g)△H=-Q2 kJ•mol-1
③2C(s)+2H2(g)?C2H4(g)△H=-Q3 kJ•mol-1
其中2Q1、Q2、Q3,从大到小的顺序是( )
a、C2H2(g)+H2(g)?C2H4(g)
b、2CH4(g)?C2H4(g)+2H2(g)
报据上述变化.判断以下几个热化学方程式:
①C(s)+2H2(g)?CH4(g)△H=-Q1 kJ•mol-1
②2C(s)+H2(g)?C2H2(g)△H=-Q2 kJ•mol-1
③2C(s)+2H2(g)?C2H4(g)△H=-Q3 kJ•mol-1
其中2Q1、Q2、Q3,从大到小的顺序是( )
| A. | 2Q1>Q3>Q2 | B. | Q3>Q2>2Q1 | C. | Q2>Q3>2Q1 | D. | Q3>2Q1>Q2 |
13.配制一定体积,一定物质的量浓度溶液时,下列情况中溶液的浓度偏小的是( )
| A. | 溶解后,溶液未经冷却,立即转移至容量瓶 | |
| B. | 胶头滴管滴加蒸馏水时,不小心把少量的蒸馏水滴到容量瓶外 | |
| C. | 转移溶液后,未洗涤烧杯和玻璃棒就直接定容 | |
| D. | 定容时,俯视刻度线 |
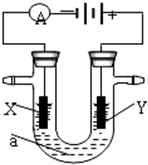 变”)
变”)