题目内容
1.已知酸性H2SO3>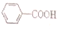 >H2CO3
>H2CO3 >HCO3-,现要将
>HCO3-,现要将 转变为
转变为 ,可行的方法是( )
,可行的方法是( )| A. | 与足量的NaOH溶液共热,再通入CO2 | |
| B. | 加稀硫酸共热后,再加入足量NaOH溶液 | |
| C. | 加热该物质溶液,再通入足量的SO2 | |
| D. | 与稀硫酸共热后,加入足量的Na2CO3 |
分析 要将 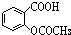 转变为
转变为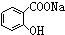 ,
,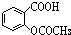 应先在碱性条件下水解生成
应先在碱性条件下水解生成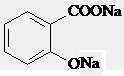 ,
,
由于酸性关系: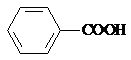
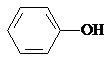
 ,据此进行分析.
,据此进行分析.
解答 解:A.与足量NaOH溶液共热,水解生成 ,再通入足量的CO2,由于酸性
,再通入足量的CO2,由于酸性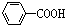 >H2CO3>
>H2CO3>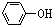 >HCO3-,生成
>HCO3-,生成 ,故A正确;
,故A正确;
B.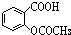 在酸性条件下水解生成
在酸性条件下水解生成 ,加入NaOH后生成
,加入NaOH后生成 ,得不到
,得不到 ,故B错误;
,故B错误;
C.加热该物质溶液,再通入足量的SO2生成 ,故C错误;
,故C错误;
D.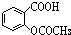 在酸性条件下水解生成
在酸性条件下水解生成 ,再加入足量Na2CO3溶液生成
,再加入足量Na2CO3溶液生成 ,得不到
,得不到 ,故D错误;
,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、羧酸性质的考查,注意酸性的比较及应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列物质中属于有机物的是( )
①酒精;②食盐;③一氧化碳;④甲烷;⑤红糖;⑥石灰石.
①酒精;②食盐;③一氧化碳;④甲烷;⑤红糖;⑥石灰石.
| A. | ①②④⑤ | B. | ①④⑤ | C. | ①③⑤ | D. | ①⑤⑥ |
10.下列各组中两个变化所发生的反应,属于同一类型的是( )
①由乙烯制取乙烷,由乙烷制溴乙烷;
②乙烯使溴水褪色,乙炔使酸性高锰酸钾水溶液褪色;
③由乙烯制聚乙烯,由乙炔制聚乙炔;
④由乙烯制取氯乙烷,由乙炔制取氯乙烯.
①由乙烯制取乙烷,由乙烷制溴乙烷;
②乙烯使溴水褪色,乙炔使酸性高锰酸钾水溶液褪色;
③由乙烯制聚乙烯,由乙炔制聚乙炔;
④由乙烯制取氯乙烷,由乙炔制取氯乙烯.
| A. | 只有②③ | B. | 只有③④ | C. | 只有①③ | D. | 只有①④ |
9.下列有关叙述:①非金属单质N能从M的化合物中置换出非金属单质M;②M原子比N原子容易得到电子;③Na-的还原性强于Mb-;④单质熔点M>N.能说明非金属元素M比N的非金属性强的是( )
| A. | ①② | B. | ②③ | C. | ②③④ | D. | ③④ |
6.下列物质属于纯净物的是( )
| A. | 聚乙烯 | B. | 冰醋酸 | C. | 福尔马林 | D. | 碘酒 |
13.X、Y、Z、W、R五种短周期主族元素周期表中的位置如图所示,下列有关说法正确的是( )
| X | Y | ||
| Z | W | R |
| A. | 原子半径的大小顺序:Z>X>Y | |
| B. | W、Y的气态氢化物的稳定性:W>Y | |
| C. | Z单质一定是金属铝 | |
| D. | W、R的最高价氧化物对应水化物的酸性:W>R |
11.下列各组离子中能大量共存,且溶液为无色透明的是( )
| A. | K+、Cu2+、Cl-、AlO2- | B. | Na+、Al3+、NO3-、HCO3- | ||
| C. | Na+、H+、NO3-、SO42- | D. | Ca2+、Cl-、CO32-、NH4+ |
 短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,A的简单离子半径是同周期元素简单离子中半径最小的.请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,A的简单离子半径是同周期元素简单离子中半径最小的.请回答下列问题: .
. .该阳离子中存在的化学键有共价键,写出该阳离子与F氢化物的水溶液反应的离子方程式:2H2O++H2S=S↓+2H2O+2H+.
.该阳离子中存在的化学键有共价键,写出该阳离子与F氢化物的水溶液反应的离子方程式:2H2O++H2S=S↓+2H2O+2H+.
 ,F
,F .
. .
.