��Ŀ����
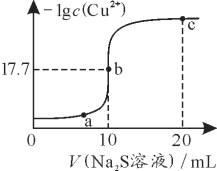
����Ŀ��ij�¶��£���10 mL 0.1 mol��L��1 CuCl2��Һ�еμ�0.1 mol��L��1��Na2S��Һ���μӹ����У�lg c(Cu2��)��Na2S��Һ����Ĺ�ϵ��ͼ��ʾ�������й�˵����ȷ����
��֪��Ksp(ZnS)��3��10��25
A. Na2S��Һ�У�c(S2��)��c(HS��)��c(H2S)��2c(Na��)
B. a��b��c�����Ӧ����Һ�У�ˮ�ĵ���̶�����Ϊb��
C. ���¶��£�Ksp(CuS)��1��10��35.4
D. ��100 mL Zn2����Cu2�����ʵ���Ũ�Ⱦ�Ϊ0.1mol��L��1�Ļ����Һ����μ���10��3 mol��L��1��Na2S��Һ��Zn2���ȳ���
���𰸡�C
��������
��10mL0.1mol/LCuCl2��Һ�еμ�0.1mol/L��Na2S��Һ��������Ӧ��Cu2++S2-=CuS����Cu2+�������ڻ�S2-�������ھ���ˮ�⣬ˮ��ٽ�ˮ�ĵ��룬���ͼ������ܶȻ���������Һ�е��غ�˼�룬�ݴ��жϷ�����
��10mL0.1mol/LCuCl2��Һ�еμ�0.1mol/L��Na2S��Һ��������Ӧ��Cu2++S2-=CuS����Cu2+�������ڻ�S2-�������ھ���ˮ�⣬ˮ��ٽ�ˮ�ĵ��룬b����Һʱ�μ�Na2S��Һ�������10mL����ʱǡ������CuS������CuS���ڳ����ܽ�ƽ�⣺CuS��s��![]() Cu2+��aq��+S2-��aq������֪��ʱ-lgc��Cu2+��=17.7����ƽ��ʱc��Cu2+��=c��S2-��=10-17.7mol/L��
Cu2+��aq��+S2-��aq������֪��ʱ-lgc��Cu2+��=17.7����ƽ��ʱc��Cu2+��=c��S2-��=10-17.7mol/L��
A��Na2S��Һ�У����������غ㣬2c(S2��)��2c(HS��)��2c(H2S)��c(Na��)����A����
B��Cu2+�������ڻ�S2-�������ھ���ˮ�⣬ˮ��ٽ�ˮ�ĵ��룬b��ʱǡ���γ�CuS��������ʱˮ�ĵ���̶Ȳ�����a��b��c���������ģ���B����
C�����¶��£�ƽ��ʱc��Cu2+��=c��S2-��=10-17.7mol/L����Ksp��CuS��=c��Cu2+��![]() c��S2-��=10-17.7mol/L��10-17.7mol/L=10-35.4mol2/L2����C��ȷ��
c��S2-��=10-17.7mol/L��10-17.7mol/L=10-35.4mol2/L2����C��ȷ��
D����100mLZn2+��Cu2+Ũ�Ⱦ�Ϊ0.1mol��L��1�Ļ����Һ����μ���10��3 mol��L��1��Na2S��Һ������ZnSʱ��Ҫ��S2-Ũ��Ϊc��S2-��=![]() =
=![]() mol/L=3��10-24mol/L��
mol/L=3��10-24mol/L��
����CuSʱ��Ҫ��S2-Ũ��Ϊc��S2-��=![]() =
=![]() mol/L=10-34.4mol/L�������CuS��������S2-Ũ�ȸ�С�����Ȳ���CuS��������D����
mol/L=10-34.4mol/L�������CuS��������S2-Ũ�ȸ�С�����Ȳ���CuS��������D����
��ѡC��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�