题目内容
4.下表列出了有关晶体的说明,其中有错误的是| 选项 | ||||
| 晶体名称 | 碘化钾 | 干冰 | 氖 | 二氧化硅 |
| 组成晶体的微粒名称 | 阴、阳离子 | 分子 | 原子 | 原子 |
| 晶体内存在的结合力 | 离子键 | 范德华力 | 共价键 | 共价键 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碘化钾为离子晶体,组成微粒为离子,存在离子键;
B.干冰为分子晶体,存在分子间作用力;
C.氖晶体为分子晶体,且为单原子分子,晶体内存在的作用力为范德华力;
D.二氧化硅为原子晶体,组成微粒为原子,以共价键相结合.
解答 解:A.碘化钾为离子晶体,组成微粒为离子,组成晶体粒子间的结合力为离子键,故A正确;
B.干冰为分子晶体,组成微粒为分子,分子之间的结合力为范德华力,也叫做分子间作用力,故B正确;
C.氖晶体属于分子晶体,其晶体内存在的作用力为范德华力,不是共价键,故C错误;
D.二氧化硅为原子晶体,组成微粒为原子,组成晶体粒子间的结合力为共价键相,故D正确;
故选C.
点评 本题考查晶体的结构、组成以及微粒间作用力,题目难度不大,明确常见晶体的类型及含有微粒间作用力为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
15.在密闭容中发生下列反应aA(g)?cC(g)+dD(g)△H=-m kJ/mol达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.7倍,下列叙述正确的是( )
| A. | 平衡向正反应方向移动了 | B. | A的转化率变大了 | ||
| C. | a<c+d | D. | △H值变大了 |
12.NH3 分子的空间构型是三角锥形,而不是正三角形的平面结构,解释该事实的充分理由是( )
| A. | NH3分子是极性分子 | |
| B. | 分子内3个N-H键的键长相等,键角相等 | |
| C. | NH3分子内3个N-H键的键长相等,3个键角都等于107° | |
| D. | NH3分子内3个N-H键的键长相等,3个键角都等于120° |
19.下列说法错误的是( )
| A. | 将22.4LHCl气体溶于水配成1L溶液,溶质的物质的量浓度为1 mol•L-1 | |
| B. | 配制0.5L 0.1 mol•L-1的NaOH溶液,需要称量氢氧化钠固体2.0g | |
| C. | 0.5 L 2 mol•L-1的氯化钡溶液中,钡离子和氯离子总数为1.806×1024 | |
| D. | 密度为0.91 g•cm-3的氨水,质量分数为25%,加等体积的水稀释后,所得溶液的质量分数小于12.5% |
9.配制一定物质的量浓度的溶液时,会导致所配溶液浓度偏大的操作是( )
| A. | 在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中 | |
| B. | 定容摇匀后,发现液面低于刻度线,又加水到刻度线 | |
| C. | 用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理 | |
| D. | 定容时俯视刻度线 |
13.下列化学用语正确的是( )
| A. | 小苏打的化学式:NaHCO3 | |
| B. | Cl原子的结构示意图: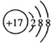 | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | 硫酸的电离方程式:H2SO4=H2++SO42- |
14.具备基本的化学实验技能是进行科学探究的基本保证.下列实验操作中正确的是( )
| A. | 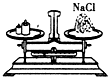 称取食盐 | B. | 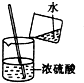 稀释浓硫酸 | C. | 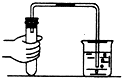 检查气密性 | D. |  点燃酒精灯 |