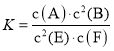题目内容
【题目】向800mL稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出NO气体![]() 标准状况
标准状况![]() ,同时溶液质量增加
,同时溶液质量增加![]() ,下列判断正确的是
,下列判断正确的是![]()
A.原溶液中投入铁粉物质的量是![]()
B.原溶液中的![]() 浓度是
浓度是![]()
C.反应后的溶液中![]() :
:![]() :1
:1
D.反应后的溶液中还可以溶解![]() 铜
铜
【答案】C
【解析】
生成NO的物质的量为![]() =0.5mol,
=0.5mol,
设生成Fe2+、Fe3+的物质的量分别为xmol、ymol,
由溶液质量增重18.6g,则:(x+y)mol×56g/mol-0.5mol×30g/mol=18.6g,
由电子转移守恒,则:2xmol+3ymol=0.5mol×3,
联立方程,解得x=0.3、y=0.3,
反应后c(Fe2+):c(Fe3+)为=0.3:0.3=1:1,
A.原溶液中投入铁粉物质的量是0.3mol+0.3mol=0.6mol,选项A错误;
B.根据N元素守恒:n(HNO3)=2n(Fe2+)+3n(Fe3+)+n(NO)=2×0.3mol+3×0.3mol+0.5mol=2mol,c(HNO3)=![]() =2.5mol/L,选项B错误;
=2.5mol/L,选项B错误;
C.由以上计算可知反应后的溶液中c(Fe2+):c(Fe3+)=1:1,选项C正确;
D.由反应2Fe3++Cu=2Fe2++Cu2+可知,还可溶解0.15molCu,质量为0.15mol×64g/mol=9.6g,选项D错误。
答案选C。

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目