ЬтФПФкШн
ЁОЬтФПЁП25ЁцЪБЃЌAgClЕФKsp=1.8ЁС10-10ЃЌAg2CO3дкЫЎжаЕФГСЕэШмНтЦНКтЧњЯпШчЭМЫљЪОЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧЃЈ ЃЉ
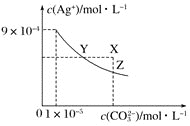
A.Ag2CO3ЕФKspЮЊ8.1ЁС10-12
B.Ag2CO3(s)+2Cl-(aq)![]() 2AgCl(s)+CO32-(aq)ЕФЦНКтГЃЪ§K=2.5ЁС108
2AgCl(s)+CO32-(aq)ЕФЦНКтГЃЪ§K=2.5ЁС108
C.ЯђAg2CO3ЕФБЅКЭШмвКжаМгШыK2CO3(s)ЃЌПЩЪЙc(CO32-)діДѓ(гЩYЕуЕНXЕу)
D.ЯђЭЌХЈЖШЕФKClКЭK2CO3ЕФЛьКЯШмвКжаЕЮШы0.001molЁЄL-1AgNO3ШмвКЃЌCO32-ЯШГСЕэ
ЁОД№АИЁПCD
ЁОНтЮіЁП
A. Ag2CO3ЕФШмЖШЛ§Ksp=c2(Ag+)ЁСc(CO32)=(9ЁС104)2ЁС(1ЁС105)=8.1ЁС1012ЃЌЙЪAе§ШЗЃЛ
B. ИУЗДгІЕФЦНКтГЃЪ§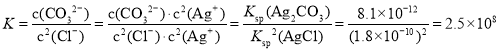 ЃЌЙЪBе§ШЗЃЛ
ЃЌЙЪBе§ШЗЃЛ
C. МгШыK2CO3(s)КѓЃЌAg2CO3ГСЕэШмНтЦНКте§ЯђвЦЖЏЃЌШмвКжаc(CO32)діДѓЃЌc(Ag+)МѕаЁЃЌЖјYЕНXЕФвЦЖЏЙ§ГЬжаc(Ag+)ВЛБфЃЌЙЪCДэЮѓЃЛ
D. аЮГЩAgClГСЕэЫљашClХЈЖШ![]() ЃЌаЮГЩAg2CO3ГСЕэЫљашCO32ХЈЖШ
ЃЌаЮГЩAg2CO3ГСЕэЫљашCO32ХЈЖШ![]() ЃЌвђДЫClЯШаЮГЩГСЕэЃЌЙЪDДэЮѓЁЃ
ЃЌвђДЫClЯШаЮГЩГСЕэЃЌЙЪDДэЮѓЁЃ
злЩЯЫљЪіЃЌД№АИЮЊCDЁЃ

СЗЯАВсЯЕСаД№АИ
ЯрЙиЬтФП