题目内容
(14分)二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛。
(1)①TiCl4水解生成TiO2·xH2O的化学方程式为 。
②检验TiO2·xH2O中Cl-是否被除净的方法是 。
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:
(2)Fe2O3与H2SO4反应的离子方程式是 。
(3)甲溶液中除含TiO2+之外还含有的金属阳离子有 。
(4)加Fe的作用是 。
Ⅱ、二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:
TiO2 TiCl4
TiCl4 Ti
Ti
反应②的方程式是 ,该反应需要在Ar气氛中进
行,请解释原因: 。
(14分,每空2分)
(1)①TiCl4 + (x + 2)H2O(过量) TiO2·xH2O↓ + 4HCl(写=不扣分)
TiO2·xH2O↓ + 4HCl(写=不扣分)
②取少量水洗液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已洗净。
(2)Fe2O3 + 6H+ = 2Fe3+ + 3H2O
(3)Fe3+、Fe2+
(4)将Fe3+转化为Fe2+
(5)TiCl4 + 2Mg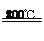 2MgCl2 + Ti;防止高温下Mg(Ti)与空气中O2(或CO2、N2)作用。
2MgCl2 + Ti;防止高温下Mg(Ti)与空气中O2(或CO2、N2)作用。
解析试题分析:(1)①TiCl4水解生成TiO2·xH2O和氯化氢,根据元素守恒规律书写其化学方程式为
TiCl4 + (x + 2)H2O(过量) TiO2·xH2O↓ + 4HCl;
TiO2·xH2O↓ + 4HCl;
②检验沉淀是否被洗干净的方法是取少量洗涤后的溶液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已洗净。
(2)Fe2O3与H2SO4发生反应生成硫酸铁和水,氧化铁是氧化物,不能拆开,硫酸是强酸,写成离子形式,所以离子方程式为Fe2O3 + 6H+ = 2Fe3+ + 3H2O ;
(3)FeTiO3中Ti元素化合价为+4价,则Fe为+2价,钛铁矿中含有氧化铁,所以甲溶液中除iO2+之外还含有的金属阳离子有Fe3+、Fe2+
(4)加Fe的作用是将Fe3+转化为Fe2+,便于Fe2+结晶为FeSO4·7H2O
(5)TiCl4与Mg在800℃发生置换反应生成钛和氯化镁,化学方程式为TiCl4 + 2Mg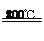 2MgCl2 + Ti;
2MgCl2 + Ti;
Mg与Ti在高温条件下易与空气中的氧气、二氧化碳发生反应,所以为了防止高温下Mg(Ti)与空气中O2(或CO2、N2)作用,该反应需要在Ar气氛中进行。
考点:考查工业制备钛、二氧化钛的反应原理,对工业流程的分析,化学方程式的书写

下列离子方程式中,正确的
| A.在AlCl3溶液中加入过量氨水:Al3+ + 3NH3·H2O =Al(OH)3↓ + 3NH4+ |
| B.大理石加入过量盐酸中:CO32-+2H+= CO2↑+H2O |
| C.稀硫酸和Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D.在CuSO4溶液中加入Ba(OH)2溶液:Ba2+ + SO42- =BaSO4↓ |
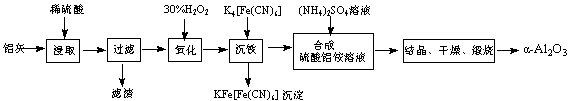
(14分)氧化锌是橡胶、油漆、搪瓷、电缆、医药、电子、化学等工业的重要原料。以氧
化锌粗品为原料制备活性氧化锌的生产工艺流程如下: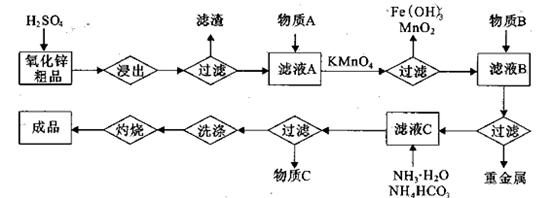
(1).浸出”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+、 +、Mn2+等
+、Mn2+等
杂质。物质A的作用是调节溶液的pH至5 4,物质A最好选择________。
| A.NH3.H2O | B.Na2CO3 | C.H2SO4 | D.ZnO |

该温度下
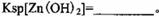 。
。(2) KMnO4的作用是除去Mn2+和Fe2+,则KMnO4与Mn2+反应的离子方程式为_____________________________________;若溶液中
 ,则处理1
,则处理1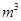 该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。
该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。(3)杂质Cu2+、
 2+可利用置换反应除去,则物质B是_________。
2+可利用置换反应除去,则物质B是_________。(4)被灼烧的沉淀是
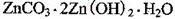 ,生成该沉淀的化学方程式为________。
,生成该沉淀的化学方程式为________。如何检验该沉淀是否洗净?________________________________。
有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、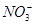 、
、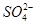 、Cl-、I-、
、Cl-、I-、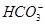 ,取该溶液进行如下实验:
,取该溶液进行如下实验:
| 实验步骤 | 实验现象 |
| ①取少量该溶液,加几滴甲基橙溶液 | 溶液变红色 |
| ②取少量该溶液,加入铜片和浓硫酸,加热 | 有无色气体产生,遇空气可以变成红棕色 |
| ③取少量该溶液,加入BaCl2溶液 | 有白色沉淀生成 |
| ④取③中的上层清液,加入AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| ⑤取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
(1)溶液中一定存在的离子是 ;溶液中肯定不存在的离子是 。
(2)为进一步确定其他离子,应该补充的实验及对应欲检验离子的名称(若为溶液反应,说明使用试剂的名称,不必写详细步骤) 。
(3)写出实验⑤中所有反应的离子方程式: 。
有一无色透明的溶液,要确定是否含有以下离子:H+、K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下:
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴紫色石蕊溶液 | 溶液变红色 |
| (2)取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| (4)取(3)中上层清液,加AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
由此判断:
(1)溶液中肯定存在的离子是 ,溶液中肯定不存在的离子是 。
(2)为进一步确定其他离子,应该补充的实验及对应欲检离子的名称(如为溶液反应,说明使用试剂的名称,不必写详细操作步骤)。 。
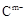 、
、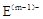 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题: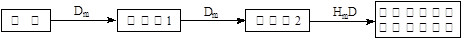
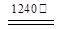 2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
