题目内容
10.下列实验操作中,正确的是( )| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | |
| C. | 鉴别己烯和苯:向己烯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色 | |
| D. | 除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质可以是H2O、Ba(OH)2、HCl、Na2CO3 |
分析 A.苯与溴水不反应;
B.应先加入浓硝酸,最后加入浓硫酸;
C.己烯与酸性高锰酸钾发生氧化还原反应;
D.Ba(OH)2除去Mg2+、SO42-,Na2CO3除去Ca2+及过量的Ba2+,HCl在最后.
解答 解:A.制取溴苯应用液溴,不能用溴水,故A错误;
B.为防止酸液的飞溅,应先加入浓硝酸,最后加入浓硫酸,故B错误;
C.己烯与酸性高锰酸钾发生氧化还原反应而使高锰酸钾溶液褪色,苯与高锰酸钾不反应,可鉴别,故C正确;
D.除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质可以是H2O、Ba(OH)2、Na2CO3、HCl,HCl可除去过量的Na2CO3,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及溴苯、硝基苯的制备以及有机物的鉴别、粗盐提纯等,把握物质的性质及反应原理为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
20.在相同条件下,取相同体积的下列各物质,其充分燃烧后生产二氧化碳和水的物质的量最多的是( )
| A. | C2H6 | B. | C3H6 | C. | C3H8 | D. | C2H4 |
18.下列各选项陈述I和陈述II均正确且二者有因果关系的是( )
| 陈述I | 陈述II | |
| A | 二氧化硫使高锰酸钾溶液褪色 | 二氧化硫具有漂白性 |
| B | 铁与高温水蒸气能反应 | 四氧化三铁可以作为颜料 |
| C | 同一周期从左至右核电荷数增大 | 同一周期主族元素从左至右原子半径减小 |
| D | 经过打磨的铝片与盐酸反应速率由慢到快 | 铝片与盐酸反应是放热反应 |
| A. | A | B. | B | C. | C | D. | D |
5.如图是氯气的制备以及氯、溴、碘的非金属性比较实验,充分反应一段时间后,打开装置D的活塞,将装置D中少量溶液加入装置E中,振荡,观察实验现象,下列说法正确的是( )
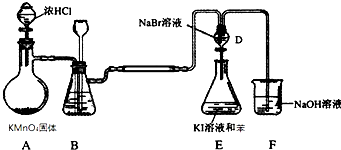

| A. | 装置E下层呈现紫红色 | |
| B. | 装置B中可盛放水吸收氯气中的HCl气体 | |
| C. | F2不能与NaCl溶液反应置换出氯气 | |
| D. | 装置E中有机试剂层呈现紫红色,能说明非金属性Br>I |
15.磷酸铁锂电池应用广泛.该锂电池将锂嵌入碳材料,含Li+导电固体为电解质;电解质中迁移介质是一种有机聚合物,其单体之一M结构简式如图:电池反应为:LiC6+FePO4$?_{充电}^{放电}$LiFePO4+6C,下列说法正确的是( )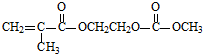
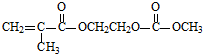
| A. | 放电时,体系中的Li+向负极移动 | |
| B. | 放电时,FePO4作正极发生氧化反应 | |
| C. | 充电时,与电源正极相连的电极反应为:LiFePO4-e-═Li++FePO4 | |
| D. | 1 mol有机物M与足量NaOH溶液反应,消耗2 mol NaOH |
2.下列离子方程式不正确的是( )
| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 金属钾与水反应:2K+2H2O═2K++2OH-+H2↑ | |
| C. | 氧化铝溶于NaOH溶液:Al2O3+2OH-═2AlO2-+H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
20.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 常温下,1mol Fe与足量稀HNO3反应,转移电子的数目为2NA | |
| B. | 18gD2O中含有的质子数目为10NA | |
| C. | 标准状况下,22.4L二氯甲烷的分子数约为NA | |
| D. | 28g由C2H4和C3H6组成的混合物中含有氢原子的数目为4NA |
