题目内容
2.下列离子方程式不正确的是( )| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 金属钾与水反应:2K+2H2O═2K++2OH-+H2↑ | |
| C. | 氧化铝溶于NaOH溶液:Al2O3+2OH-═2AlO2-+H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
分析 A.醋酸为弱酸,离子方程式中不能拆开;
B.钾与水反应生成氢氧化钾和氢气;
C.氧化铝为两性氧化物,与氢氧化钠溶液反应生成偏铝酸钠和水;
D.偏铝酸钠与过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠.
解答 解:A.碳酸钙与醋酸的反应中,碳酸钙和醋酸都不能拆开,正确的离子反应为:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑,故A错误;
B.金属钾与水反应生成氢氧化钾和氢气,反应的离子方程式为:2K+2H2O═2K++2OH-+H2↑,故B正确;
C.氧化铝溶于NaOH溶液,反应生成偏铝酸钠和水,反应的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,故C正确;
D.NaAlO2溶液中通入过量CO2,反应生成氢氧化铝沉淀,反应的离子方程式为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故D正确;
故选A.
点评 本题考查了离子方程式的书写判断,为高考中的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
12.下列关于卤代烃的叙述中正确的是( )
| A. | 所有卤代烃都是难溶于水,密度比水小的液体 | |
| B. | 所有卤代烃在适当条件下都能发生消去反应 | |
| C. | 所有卤代烃都含有卤原子 | |
| D. | 所有卤代烃都是通过取代反应制得的 |
13.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,则( )
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 分子中可能含有氧原子 | D. | 有机物的分子式为CH4Ox(x=O、1) |
10.下列实验操作中,正确的是( )
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | |
| C. | 鉴别己烯和苯:向己烯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色 | |
| D. | 除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质可以是H2O、Ba(OH)2、HCl、Na2CO3 |
7.下列物质中既含有离子键又含有共价键的是( )
| A. | Na2O | B. | MgCl2 | C. | CH3COOH | D. | NaOH |
14.将SO2和18O2充入反应容器,当反应达到平衡时,18O原子将( )
| A. | 存在于氧气和三氧化硫中 | B. | 只存在于三氧化硫中 | ||
| C. | 三种物质中都有 | D. | 无法判断 |
11.下列物质中,在一定条件下既能发生加成反应,也能发生取代反应,但不能使KMnO4酸性溶液褪色的是
( )
( )
| A. | 乙烷 | B. | 苯 | C. | 乙烯 | D. | 乙醇 |
12.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 31g白磷中含有的共价键数目为1.5NA | |
| B. | 0.1L3.0mol•L-1的NH4N03溶液中含有的NH4+的数目为0.3NA | |
| C. | 标准状况下,22.4L己烷中含共价键数目为19NA | |
| D. | 常温常压下,lmolCl2与足量的水充分反应,转移的电子数目为NA |
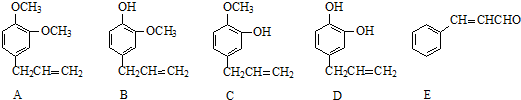
 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$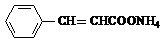 +H2O+2Ag↓+3NH3,Y的结构简式为
+H2O+2Ag↓+3NH3,Y的结构简式为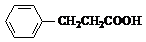 ,反应③属于加成反应.
,反应③属于加成反应.