题目内容
15.磷酸铁锂电池应用广泛.该锂电池将锂嵌入碳材料,含Li+导电固体为电解质;电解质中迁移介质是一种有机聚合物,其单体之一M结构简式如图:电池反应为:LiC6+FePO4$?_{充电}^{放电}$LiFePO4+6C,下列说法正确的是( )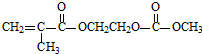
| A. | 放电时,体系中的Li+向负极移动 | |
| B. | 放电时,FePO4作正极发生氧化反应 | |
| C. | 充电时,与电源正极相连的电极反应为:LiFePO4-e-═Li++FePO4 | |
| D. | 1 mol有机物M与足量NaOH溶液反应,消耗2 mol NaOH |
分析 A.放电时,电解质溶液中阳离子向正极移动,阴离子向负极移动;
B.放电时,Fe元素化合价由+3价变为+2价;
C.充电时,与电源正极相连的电极是阳极,阳极上失电子发生氧化反应;
D.该物质中酯基水解生成的羧基和碳酸都能和氢氧化钠发生反应.
解答 解:A.放电时,电解质溶液中阳离子向正极移动,阴离子向负极移动,所以放电时,体系中的Li+向正极移动,故A错误;
B.放电时,Fe元素化合价由+3价变为+2价,所以Fe元素得电子发生还原反应,故B错误;
C.充电时,与电源正极相连的电极是阳极,阳极上失电子发生氧化反应,电极反应式为LiFePO4-e-═Li++FePO4,故C正确;
D.该物质中酯基水解生成的羧基和碳酸都能和氢氧化钠发生反应,所以1 mol有机物M与足量NaOH溶液反应,消耗3mol NaOH,故D错误;
故选C.
点评 本题考查化学电源新型电池及有机物结构和性质,明确化学电源中各个电极上发生的反应是解本题关键,难点是电极反应式的书写,注意D中该物质水解生成碳酸,为易错点.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
6.下列说法不正确的是( )
| A. | 反应热可分为多种,如燃烧热、中和热、溶解热等 | |
| B. | 氢气是一种燃烧热高,来源丰富,环保的一级能源 | |
| C. | 达化学平衡时,同一物质的正反应速率一定等于其逆反应速率 | |
| D. | 由自由能判据推出反应2CO(g)═2C(s)+O2(g)在任何温度下都不能自发进行 |
3.四种主族元素的离子aXm+、bYn+、cZn-和 dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则下列叙述的判断正确的是( )
①a-b=n-m ②元素的原子序数a>b>c>d ③元素非金属性Z>R ④最高价氧化物对应水化物碱性X>Y.
①a-b=n-m ②元素的原子序数a>b>c>d ③元素非金属性Z>R ④最高价氧化物对应水化物碱性X>Y.
| A. | 只有②③正确 | B. | 只有③正确 | C. | ①②③④都正确 | D. | 只有①②③正确 |
10.下列实验操作中,正确的是( )
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | |
| C. | 鉴别己烯和苯:向己烯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色 | |
| D. | 除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质可以是H2O、Ba(OH)2、HCl、Na2CO3 |
20.下列四种盐酸跟锌片反应,起始时反应速率最快的是( )
| A. | 10℃20 mL 3 mol/L的盐酸 | B. | 10℃40 mL 2 mol/L的盐酸 | ||
| C. | 20℃20 mL 2 mol/L的盐酸 | D. | 20℃10 mL 4 mol/L的盐酸 |
7.下列物质中既含有离子键又含有共价键的是( )
| A. | Na2O | B. | MgCl2 | C. | CH3COOH | D. | NaOH |
4.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 氢氧化钠溶液与稀盐酸混合 | |
| B. | 氢氧化钡晶体与氯化铵晶体混合搅拌 | |
| C. | 乙醇燃烧 | |
| D. | 铝热反应 |
5.下列属于复分解反应的是( )
| A. | NH4HCO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑ | |
| B. | C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O | |
| C. | 3Cl2+6NaOH═5NaCl+NaClO3+3H2O | |
| D. | 2HCl+CaCO3═CaCl2+CO2↑+H2O |
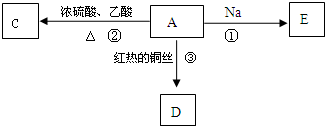 A是化学实验室中最常见的有机物,易溶于水有特殊香味,并能进行如图所示的多种反应.
A是化学实验室中最常见的有机物,易溶于水有特殊香味,并能进行如图所示的多种反应.