题目内容
17.下列除杂方法不正确的是( )| 物质 | 杂质 | 试剂或材料 | 操作 | |
| A | 淀粉溶液 | NaCl | 半透膜 | 渗析 |
| B | 苯 | 苯酚 | 浓溴水 | 过滤 |
| C | 乙醇 | 水 | 生石灰 | 蒸馏 |
| D | 乙酸乙脂 | 乙醇 | 饱和Na2C03溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.淀粉溶液为胶体,淀粉不能透过半透膜;
B.溴、三溴苯酚易溶于苯;
C.水与生石灰发生反应生成氢氧化钙,可增大沸点差;
D.乙酸乙酯不溶于饱和碳酸钠溶液,乙醇易溶于水.
解答 解:A.淀粉溶液为胶体,淀粉不能透过半透膜,可用渗析的方法分离,故A正确;
B.苯酚与溴反应生成氨溴苯酚,溴、三溴苯酚易溶于苯,应用氢氧化钠溶液分离,故B错误;
C.水与生石灰发生反应生成氢氧化钙,蒸馏可分离,故C正确;
D.乙酸乙酯不溶于饱和碳酸钠溶液,乙醇易溶于水,可用饱和碳酸钠溶液分离,故D正确.
故选B.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,为解答该题的关键,注意把握实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
7.“绿色化学”是当今社会提出的一个新概念.在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%.以下反应最符合绿色化学概念的是( )
| A. | 乙烯聚合为聚乙烯高分子材料 | B. | 甲烷与氯气制备一氯甲烷 | ||
| C. | 以铜和浓硝酸为原料生产硝酸铜 | D. | 用二氧化硅制备高纯硅 |
8.能源可划分为一级能源和二级能源.自然界中以形成形式提供的能源称为一级能源,需依靠其他能源间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:2H2O(l)═2H2(g)+O2(g)下列叙述正确的是( )
| A. | 电源是一级能源 | B. | 天然气是一级能源 | ||
| C. | 水力是二级能源 | D. | 干馏煤气是一级能源 |
5.25℃时,下列各组离子能在指定溶液中大量共存的是( )
| A. | 无色溶液:K+、Na+、MnO4-、SO42- | |
| B. | pH=11溶液:CO32-、Na+、K+、SO32- | |
| C. | 由水电离的 c(H+)=10-12 mol•L-1,溶液:Cl-、HCO3-、NO3-、Na+ | |
| D. | 酸性溶液:Fe2、NO3-、Cl-、NH4+ |
12.在恒温密闭容器中,Z(?)+W(?)?X(g)+Y(?)反应速率随时间变化如图所示,其中t2时刻为其他条件不变,只缩小容器体积.下列有关说法中不正确的是( )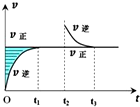

| A. | 该反应的Z和W-定不为气态 | |
| B. | t1-t2与t3-t4两时段,反应体系的气体平均摩尔质量不可能相等 | |
| C. | 该温度下,若此反应的平衡常数表达式为K=[X],则t1-t2与t3-t4两时段的c(X)相同 | |
| D. | 若在高温条件下,该反应才能自发进行,则该反应的平衡常数K随温度升高而增大 |
2.下列比较正确的是( )
| A. | 电离能:N>O>F | B. | 物质熔点:H2O>I2>CO2 | ||
| C. | 共价键的极性:C-F>C-O>C-N | D. | 氢化物的稳定性:HBr>HCl>HF |
9.下列说法错误的是( )
| A. | 氧化铝陶瓷、氮化硅陶瓷都属于新型无机非金属材料 | |
| B. | 煤矿井下的瓦斯爆炸主要是氢气燃烧引起的 | |
| C. | 乙烯的产量是衡量一个国家石油化工发展水平的标志 | |
| D. | 在粉尘较多的工作场所,工作人员易患硅肺病 |
6.已知,常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17,下列叙述中正确的是( )
| A. | 向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 | |
| B. | 向AgCl的饱和溶液中加入KCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) | |
| C. | 常温下,AgCl在饱和KCl溶液中的Ksp比在纯水中的Ksp小 | |
| D. | 将0.001 mol•L-1的AgNO3溶液滴入NaCl和NaI的混合溶液中,一定先产生AgI沉淀 |
7.欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的是( )
| A. | 乙酸乙酯(乙酸):加饱和Na2CO3 溶液,充分振荡静置后,分液 | |
| B. | 乙醇(水):加入新制生石灰,蒸馏 | |
| C. | 乙酸(乙醇):加入金属钠,蒸馏 | |
| D. | 苯(液溴):加入NaOH溶液,分液 |