题目内容
【题目】经检测某工厂的酸性废水中所含离子及其浓度如下表所示:
离子 | Fe3+ | Cu2+ | SO42- | Na+ | H+ |
浓度/(mol/L) | 2×10-3 | 1×10-3 | 1×10-2 | 2×10-3 |
(1)c(H+)= mol/L。
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4·7H2O)。

① 工业废水中加入铁粉后,反应的离子方程式为:
Fe + Cu2+ == Fe2+ + Cu、 、 。
② 试剂B是 。
③ 操作③是蒸发浓缩、冷却结晶、 ,最后用少量冷水洗涤晶体,在低温下干燥。
④ 通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是 。
⑤ 获得的FeSO4·7H2O需密闭保存,原因是 。
⑥ 上述1000 L废水经处理,可获得 FeSO4·7H2O的物质的量是 mol。
【答案】(1)0.01
(2)① Fe +2Fe3+ == 3Fe2+ Fe +2H+ == Fe2+ +H2↑ ② 硫酸 ③ 过滤
④ 取少量D中溶液于试管中,滴加1滴KSCN溶液,不出现红色,说明废水中Fe3+除尽
⑤ FeSO4有还原性,易被氧化(或FeSO4·7H2O失去结晶水)⑥ 12
【解析】
试题(1)根据电荷守恒知,c(H+)+3 c(Fe3+)+2 c(Cu2+ )+ c(Na+)= c(OH-)+2 c(SO42-),废水呈强酸性,氢氧根浓度很小,计算时可忽略,代入题给数据计算得c(H+)=0.01 mol/L;
(2) ① 工业废水中含有硫酸铜、硫酸铁和硫酸,加入铁粉后,反应的离子方程式为:Fe + Cu2+ == Fe2+ + Cu、Fe +2Fe3+ == 3Fe2+ 、Fe +2H+ == Fe2+ +H2↑。② 过滤,固体C为铁和铜的混合物,加入过量硫酸,过滤,得铜和硫酸亚铁溶液,故试剂B是硫酸。③ 操作③是从溶液中获得晶体的操作,为蒸发浓缩、冷却结晶、过滤,最后用少量冷水洗涤晶体,在低温下干燥。④Fe3+的检验用KSCN溶液,故判断废水中Fe3+是否除尽,实验方法是取少量D中溶液于试管中,滴加1滴KSCN溶液,不出现红色,说明废水中Fe3+除尽。⑤ Fe2+易被氧化,绿矾晶体易失去结晶水,故FeSO4·7H2O需密闭保存,原因是FeSO4有还原性,易被氧化(或FeSO4·7H2O失去结晶水)。⑥ 1000 L废水中n(Fe3+)=2mol,560g铁粉的物质的量为10mol,根据铁元素守恒知,经上述处理,可获得 FeSO4·7H2O的物质的量是12mol。

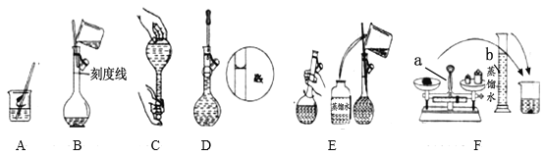
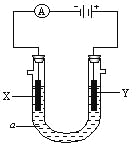
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
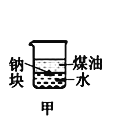
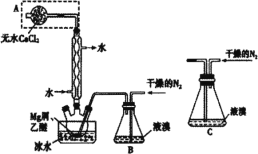
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D