题目内容
8.晶体硅是一种重要的半导体材料,工业上晶体硅的制备流程如下:石英$→_{高温}^{①}$粗硅$→_{450-500℃}^{②Cl_{2}}$$\stackrel{③精馏}{→}$高纯SiCl4$→_{高温}^{④H_{2}}$高纯硅
在高温条件下,粗硅中的杂质硼、铝、铁、磷等均能与氯气直接反应生成相应的氯化物.
有关物质物理性质:
| 物 质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
(1)写出工业上获得粗硅的化学方程式:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(2)通过精馏(类似多次蒸馏)可得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的元素是Al、P(填写元素符号).
(3)用SiCl4与过量干燥的H2反应制备纯硅,为保证制备纯硅实验的成功,除控制好反应温度外,还需确保实验装置中不能混入空气,原因是氢气与氧气爆炸,硅和氧气高温反应.
分析 (1)碳能与二氧化硅反应生成硅单质;
(2)氯气与粗硅反应生成SiCl4,精馏粗产品可得高纯度四氯化硅,由表中数据可以看出,蒸出SiCl4气体时,BCl3早已成气体被蒸出,而AlCl3、FeCl3、PCl5升华温度均低于SiCl4;
(3)Si是亲氧元素,防止Si被氧化和氢气和氧气的混合气体会发生爆炸;
解答 解:由制备四氯化硅的实验流程可知,A中发生二氧化锰与浓盐酸的反应生成氯气,B中饱和实验水除去HCl,C装置中浓硫酸干燥氯气,D中发生Si与氯气的反应生成四氯化硅,由信息可知,E装置制取氢气,F可防止倒吸,最后氢气还原SiCl4,
(1)碳能与二氧化硅反应生成硅单质,化学反应方程式:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,故答案为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(2)氯气与粗硅反应生成SiCl4,精馏粗产品可得高纯度四氯化硅,由表中数据可以看出,蒸出SiCl4气体时,BCl3早已成气体被蒸出,而AlCl3、FeCl3、PCl5升华温度均低于SiCl4,所以当SiCl4蒸出后,而AlCl3、FeCl3、PCl5还为固体留在瓶里,故答案为:Al、P;
(3)Si是亲氧元素,为防止Si被氧化,需要排尽装置中的空气,而体系中有氢气,故答案为:氢气与氧气爆炸,硅和氧气高温反应.
点评 本题以Si的制取为载体考查化学实验,涉及氧化还原反应、基本操作、混合物的分离和提纯等知识点,明确反应原理是解本题关键,再结合物质的性质分析解答,同时考查学生思维的缜密性,题目难度不大.

练习册系列答案
相关题目
3.用量筒量取液体时,某同学操作如下:量筒放平稳,面对刻度,俯视液体凹液面最低处读数为20mL,倾倒出一部分液体,又仰视液体凹液面最低处读数为10ml.这位学生取出液体的实际体积为( )
| A. | 小于10mL | B. | 10mL | C. | 大于10mL | D. | 无法判断 |
13.如表是三种物质的溶解度(20℃),下列说法正确的是( )
| 物质 | MgCl2 | Mg(OH)2 | MgCO3 |
| 溶解度(g/100g) | 74 | 0.00084 | 0.01 |
| A. | 已知MgCO3的K=6.82×10-6moL-2•L-2则所含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)•c(CO32-)=6.82×10-6moL2-•L-2 | |
| B. | 将表中三种物质与水混合,加热、灼烧,最终的固体产物相同 | |
| C. | 除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3 | |
| D. | 用石灰水处理含有Mg2+和HCO3的硬水,发生的离子反应的方程式为Mg2++2HCO3+Ca2+2OH═CaCO3↓+MgCO3↓+2H2O |
20.分类是化学学习和研究中的常用手段.下列分类依据和结论都正确的是( )
| A. | NaF、MgO、CaCl2均由活泼金属和活泼非金属作用形成,都是化合物 | |
| B. | HCl、NaOH、SO3、KNO3溶于水后都能导电,它们都是电解质 | |
| C. | H2O、HCOOH、Cu(NH3)4SO4中均含有氧,都是氧化物 | |
| D. | CO(NH2)2、(NH4)2SO4、HNO3中都含有氮元素,它们都是常用的氮肥 |
17.在实验室中,对下列事故或药品的处理正确的是( )
| A. | 做完白磷燃烧实验后,剩余的白磷放入废物缸 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 做完钠与水反应的实验后,余下的钠放回原瓶 |
18.为了证明长期暴露在空气中的氢氧化钠浓溶液已经部分变质,某同学先取2mL试样于试管中,然后进行如下实验,其中不能达到目的是( )
| A. | 加入适量盐酸,观察现象 | B. | 加入澄清石灰水,观察现象 | ||
| C. | 加入氯化钡溶液,观察现象 | D. | 通入适量CO2气体,观察现象 |
 、SiO
、SiO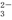 、CO
、CO 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验: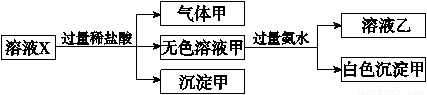
 和SiO
和SiO
 NH3·H2O
NH3·H2O