题目内容
水溶液X中只可能溶有K+、Mg2+、Al3+、AlO 、SiO
、SiO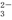 、CO
、CO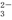 、SO
、SO 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验:
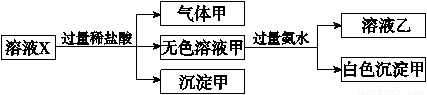
下列判断正确的是
A.白色沉淀甲是混合物
B.沉淀甲是硅酸和硅酸镁的混合物
C.K+、AlO 和SiO
和SiO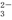 一定存在于溶液X中
一定存在于溶液X中
D.CO 和SO
和SO 一定不存在于溶液X中
一定不存在于溶液X中
练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
8.晶体硅是一种重要的半导体材料,工业上晶体硅的制备流程如下:
石英$→_{高温}^{①}$粗硅$→_{450-500℃}^{②Cl_{2}}$$\stackrel{③精馏}{→}$高纯SiCl4$→_{高温}^{④H_{2}}$高纯硅
在高温条件下,粗硅中的杂质硼、铝、铁、磷等均能与氯气直接反应生成相应的氯化物.
有关物质物理性质:
请回答下列问题:
(1)写出工业上获得粗硅的化学方程式:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(2)通过精馏(类似多次蒸馏)可得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的元素是Al、P(填写元素符号).
(3)用SiCl4与过量干燥的H2反应制备纯硅,为保证制备纯硅实验的成功,除控制好反应温度外,还需确保实验装置中不能混入空气,原因是氢气与氧气爆炸,硅和氧气高温反应.
石英$→_{高温}^{①}$粗硅$→_{450-500℃}^{②Cl_{2}}$$\stackrel{③精馏}{→}$高纯SiCl4$→_{高温}^{④H_{2}}$高纯硅
在高温条件下,粗硅中的杂质硼、铝、铁、磷等均能与氯气直接反应生成相应的氯化物.
有关物质物理性质:
| 物 质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
(1)写出工业上获得粗硅的化学方程式:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(2)通过精馏(类似多次蒸馏)可得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的元素是Al、P(填写元素符号).
(3)用SiCl4与过量干燥的H2反应制备纯硅,为保证制备纯硅实验的成功,除控制好反应温度外,还需确保实验装置中不能混入空气,原因是氢气与氧气爆炸,硅和氧气高温反应.
9.在3S+6KOH$\frac{\underline{\;\;△\;\;}}{\;}$2K2S+K2SO3+3H2O反应中,氧化剂与还原剂的质量比是( )
| A. | 2:1 | B. | 1:21 | C. | 3:1 | D. | 以上都不正确 |


 质的溶液中:①H2CO3②Na2CO3③NaHCO3④NH4HCO3⑤(NH4)2CO3下列关系或者说法正确的是
质的溶液中:①H2CO3②Na2CO3③NaHCO3④NH4HCO3⑤(NH4)2CO3下列关系或者说法正确的是 )的大小关系为②>⑤>③>④>①
)的大小关系为②>⑤>③>④>① )的大小关系为④>③>⑤>②>①
)的大小关系为④>③>⑤>②>① ,直接注入标准酸液进行滴定
,直接注入标准酸液进行滴定